 Tăng cường năng lực y tế dự phòng cho vùng biển đảo
Tăng cường năng lực y tế dự phòng cho vùng biển đảo -
 Tăng cường năng lực y tế dự phòng cho vùng biển đảo
Tăng cường năng lực y tế dự phòng cho vùng biển đảo -
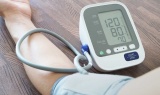 Tin mới y tế ngày 17/5: WHO cảnh báo gánh nặng tăng huyết áp toàn cầu ngày càng nghiêm trọng
Tin mới y tế ngày 17/5: WHO cảnh báo gánh nặng tăng huyết áp toàn cầu ngày càng nghiêm trọng -
 Y tế số và cuộc cách mạng dữ liệu đang thay đổi ngành y Việt Nam
Y tế số và cuộc cách mạng dữ liệu đang thay đổi ngành y Việt Nam -
 Người Việt tiêu thụ muối gần gấp đôi mức khuyến cáo của Tổ chức Y tế thế giới
Người Việt tiêu thụ muối gần gấp đôi mức khuyến cáo của Tổ chức Y tế thế giới -
Tin mới y tế ngày 16/5: Xây dựng “bộ khung chuẩn” cho bác sỹ y học cổ truyền -
TP.HCM hỗ trợ toàn diện Bệnh viện Bà Rịa, hướng tới bệnh viện cửa ngõ phía Đông Nam
Cục quản lý Dược, Bộ Y tế cho biết, hiện nay, Evusheld là thuốc, không phải là "siêu vắc-xin", chưa được cấp phép sử dụng ở đối tượng đang điều trị Covid-19, hoặc dự phòng sau phơi nhiễm Covid-19 ở những người đã tiếp xúc với trường hợp nhiễm SARS-CoV-2.
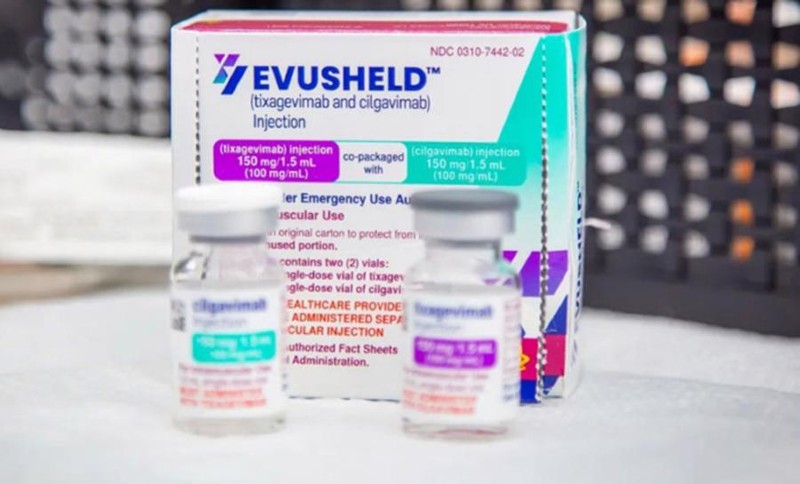 |
| Cục quản lý Dược, Bộ Y tế cho biết, hiện nay, Evusheld là thuốc, không phải là "siêu vắc-xin". |
Được biết, theo thông tin từ Cục quản lý Dược, Bộ Y tế, để đa dạng nguồn cung thuốc phòng và điều trị Covid-19, ngày 2/3, Bộ Y tế đã căn cứ các quy định hiện hành để cấp giấy phép nhập khẩu thuốc Evusheld đáp ứng nhu cầu điều trị đặc biệt của cơ sở khám chữa bệnh.
Cho đến nay, Evusheld đã được cấp phép lưu hành trong tình trạng khẩn cấp tại một số quốc gia như: Mỹ, Pháp, Các tiểu vương quốc Ả Rập thống nhất, Bahrain...
Bản chất Evusheld gồm 1 liều kháng thể đơn dòng tixagevimab và 1 liều kháng thể đơn dòng cilgavimab.
Việc sử dụng thuốc cần phải được bác sĩ đánh giá thỏa đáng và sàng lọc chặt chẽ trước khi được xác định là đối tượng sử dụng phù hợp.
Một liều thuốc được chỉ định để dự phòng mắc bệnh Covid-19 trong thời gian ít nhất 6 tháng (với các dữ liệu hiện có) cho người lớn và trẻ em từ 12 tuổi có cân nặng từ 40kg trở lên, với điều kiện các đối tượng này không đang nhiễm SARS-CoV-2 và không có tiếp xúc với người nhiễm SARS-CoV-2 được xác định và phải thuộc một trong các trường hợp sau:
Có suy giảm miễn dịch mức độ vừa đến nặng do một tình trạng bệnh lý hoặc sử dụng các thuốc hoặc phác đồ điều trị ức chế miễn dịch và có khả năng không tạo được đáp ứng miễn dịch thỏa đáng đối với vắc-xin Covid-19;
Không thể tiêm bất kỳ loại vắc-xin Covid-19 nào hiện có vì có tiền sử xảy ra tác dụng ngoại ý nghiêm trọng (ví dụ như dị ứng nặng) với bất kỳ thành phần nào của vắc-xin Covid-19.
Theo khuyến cáo của nhà sản xuất, các tình trạng y khoa hoặc phương pháp điều trị có thể dẫn tới suy giảm miễn dịch mức độ vừa đến nặng và đáp ứng miễn dịch không thỏa đáng đối với vắc-xin Covid-19 bao gồm nhưng không giới hạn:
Đang điều trị đối với các khối u đặc và bệnh lý huyết học ác tính. Cấy ghép nội tạng và đang điều trị với liệu pháp ức chế miễn dịch;
Tiếp nhận tế bào lympho T chứa thụ thể kháng nguyên dạng khảm (CAR)-T hoặc cấy ghép tế bào gốc tạo máu (trong vòng 2 năm sau khi cấy ghép hoặc đang điều trị ức chế miễn dịch);
Suy giảm miễn dịch nguyên phát mức độ vừa đến nặng (ví dụ, hội chứng DiGeorge, hội chứng Wiskott-Aldrich);
Nhiễm HIV giai đoạn tiến triển hoặc chưa được điều trị (những người nhiễm HIV với số lượng tế bào CD4 <200/mm3, tiền sử bệnh AIDS mà không được phục hồi miễn dịch, hoặc các biểu hiện lâm sàng của HIV có triệu chứng);
Điều trị tích cực bằng corticosteroid liều cao (nghĩa là ≥20 mg prednisone hoặc tương đương mỗi ngày khi dùng trong ≥ 2 tuần), tác nhân alkyl hóa, chất chống chuyển hóa, thuốc ức chế miễn dịch liên quan đến cấy ghép, tác nhân hóa trị ung thư được phân loại là ức chế miễn dịch mức độ nặng, thuốc ức chế yếu tố hoại tử khối u (TNF), và các tác nhân sinh học khác có tác dụng ức chế miễn dịch hoặc điều hòa miễn dịch (ví dụ, tác nhân ức chế tế bào B);
Hiện nay, Evusheld chưa được cấp phép sử dụng ở đối tượng đang điều trị Covid-19, hoặc dự phòng sau phơi nhiễm Covid-19 ở những người đã tiếp xúc với người nhiễm SARS-CoV-2.
Tại Việt Nam, Evusheld được cấp giấy phép nhập khẩu để sử dụng trong cơ sở khám chữa bệnh. Người bệnh phải được cơ sở khám chữa bệnh thông tin về tình trạng hồ sơ cấp phép của thuốc và cơ sở chỉ được sử dụng thuốc khi có sự đồng ý của bệnh nhân hoặc người nhà của bệnh nhân.
Như vậy, Evusheld là thuốc, không phải là "siêu vắc-xin", không được phép sử dụng Evusheld để dự phòng Covid-19 cho các đối tượng có thể tiêm vắc-xin.
Tới đây, thuốc Evusheld sẽ sớm có mặt tại Việt Nam và hệ thống Bệnh viện Đa khoa Tâm Anh là đơn vị đầu tiên đã được Bộ Y tế cấp phép chính thức sử dụng kháng thể đơn dòng Evusheld của AstraZeneca.
-
 Y tế số và cuộc cách mạng dữ liệu đang thay đổi ngành y Việt Nam
Y tế số và cuộc cách mạng dữ liệu đang thay đổi ngành y Việt Nam -
 Người Việt tiêu thụ muối gần gấp đôi mức khuyến cáo của Tổ chức Y tế thế giới
Người Việt tiêu thụ muối gần gấp đôi mức khuyến cáo của Tổ chức Y tế thế giới -
 Tin mới y tế ngày 16/5: Xây dựng “bộ khung chuẩn” cho bác sỹ y học cổ truyền
Tin mới y tế ngày 16/5: Xây dựng “bộ khung chuẩn” cho bác sỹ y học cổ truyền -
 TP.HCM hỗ trợ toàn diện Bệnh viện Bà Rịa, hướng tới bệnh viện cửa ngõ phía Đông Nam
TP.HCM hỗ trợ toàn diện Bệnh viện Bà Rịa, hướng tới bệnh viện cửa ngõ phía Đông Nam
-
Tuần Lễ Vàng 2026 - Tiếp thêm hy vọng cho các gia đình hiếm muộn -
Dịch sốt xuất huyết tăng cao, chuyên gia cảnh báo biến chứng nặng của bệnh -
Tin mới y tế ngày 15/5: Giảm nguy cơ lây bệnh lao trong cộng đồng -
Hà Nội chủ động giám sát bệnh do vi rút Hanta, phòng bệnh từ sớm, từ xa -
Imexpharm ra mắt giải pháp hỗ trợ điều trị bệnh cơ xương khớp -
Cứ sáu ca mắc não mô cầu có một ca tử vong -
Nguy cơ liệt mặt và nhầm lẫn đột quỵ trong mùa nắng nóng
-
1  Đốc thúc đưa 1 triệu tỷ đồng vào nền kinh tế; Vành đai 3 TP.HCM dư 15.750 tỷ đồng
Đốc thúc đưa 1 triệu tỷ đồng vào nền kinh tế; Vành đai 3 TP.HCM dư 15.750 tỷ đồng -
2  Đề xuất bổ sung quy hoạch tuyến cao tốc Phan Thiết - Bảo Lộc - Gia Nghĩa
Đề xuất bổ sung quy hoạch tuyến cao tốc Phan Thiết - Bảo Lộc - Gia Nghĩa -
3  Cần 24.311 tỷ đồng để thực hiện quy hoạch sân bay Cam Ranh công suất 20 triệu khách/năm
Cần 24.311 tỷ đồng để thực hiện quy hoạch sân bay Cam Ranh công suất 20 triệu khách/năm -
4  Diễn biến mới về Dự án xây dựng Vành đai 5 - Vùng Thủ đô Hà Nội
Diễn biến mới về Dự án xây dựng Vành đai 5 - Vùng Thủ đô Hà Nội
-
 EVF công bố bổ nhiệm nhân sự cấp cao
EVF công bố bổ nhiệm nhân sự cấp cao -
 Hoàng Thu Hiền: Kinh doanh món ăn gia đình bằng sự tử tế và cái tâm của người làm mẹ
Hoàng Thu Hiền: Kinh doanh món ăn gia đình bằng sự tử tế và cái tâm của người làm mẹ -
 Điều hòa Daikin FTKM cho phép tùy chỉnh độ ẩm theo nhu cầu
Điều hòa Daikin FTKM cho phép tùy chỉnh độ ẩm theo nhu cầu -
 Công bố Top 10 doanh nghiệp đổi mới sáng tạo và kinh doanh hiệu quả 2026 ngành Logistics
Công bố Top 10 doanh nghiệp đổi mới sáng tạo và kinh doanh hiệu quả 2026 ngành Logistics -
 Công bố Top 10 doanh nghiệp đổi mới sáng tạo và kinh doanh hiệu quả 2026 ngành Dược - Thiết bị y tế
Công bố Top 10 doanh nghiệp đổi mới sáng tạo và kinh doanh hiệu quả 2026 ngành Dược - Thiết bị y tế -
 Hạ tầng bứt tốc cùng vốn FDI đổ về: Đồng Nai vươn mình thành cực tăng trưởng mới
Hạ tầng bứt tốc cùng vốn FDI đổ về: Đồng Nai vươn mình thành cực tăng trưởng mới






