Tin mới y tế ngày 9/5: Trẻ dưới 6 tuổi sẽ được khám định kỳ hằng năm, có tầm soát nguy cơ tự kỷ
Tin mới y tế ngày 9/5: Trẻ dưới 6 tuổi sẽ được khám định kỳ hằng năm, có tầm soát nguy cơ tự kỷ -
 Tin mới y tế ngày 9/5: Trẻ dưới 6 tuổi sẽ được khám định kỳ hằng năm, có tầm soát nguy cơ tự kỷ
Tin mới y tế ngày 9/5: Trẻ dưới 6 tuổi sẽ được khám định kỳ hằng năm, có tầm soát nguy cơ tự kỷ -
 Người đàn ông phát hiện mắc viêm gan B mạn tính và xơ hóa gan khi kiểm tra sức khỏe định kỳ tại MEDLATEC
Người đàn ông phát hiện mắc viêm gan B mạn tính và xơ hóa gan khi kiểm tra sức khỏe định kỳ tại MEDLATEC -
 Ðại diện Việt Nam 2 năm liên tiếp thắng lớn tại Healthcare Asia Pharma Awards
Ðại diện Việt Nam 2 năm liên tiếp thắng lớn tại Healthcare Asia Pharma Awards -
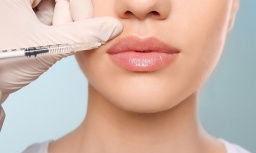
 Hoại tử, áp xe môi sau tiêm tan filler tại cơ sở làm đẹp không phép
Hoại tử, áp xe môi sau tiêm tan filler tại cơ sở làm đẹp không phép -
Chấm dứt cơn đau vai suốt 10 năm nhờ liệu pháp sinh học hiện đại -
Đề xuất thống nhất một đầu mối quản lý an toàn thực phẩm toàn quốc
Sở Y tế Hà Nội vừa có văn bản chỉ đạo gửi thủ trưởng các cơ sở y tế trên địa bàn, phòng y tế quận, huyện, thị xã, Công ty Cổ phần Dược phẩm Ampharco U.S.A, Công ty Cổ phần Dadison Hoa Kỳ có địa chỉ tại quầy 431, tầng 4, Hapu Medicenter, số 1 Nguyễn Huy Tưởng, Thanh Xuân về việc thu hồi thuốc SOS Fever® Fort không đạt tiêu chuẩn chất lượng.
.jpeg) |
| Ảnh minh họa |
Theo đó, Sở Y tế Hà Nội thông báo thu hồi trên địa bàn Hà Nội và các cơ sở đã mua lô thuốc do Công ty cổ phần Dadison Hoa Kỳ cung cấp: Viên nang mềm SOS Fever® Fort (Ibuprofen 400mg), SĐK: VN-26102-17, Số lô: B4001, NSX: 22/2/2024, HD: 22/2/2027, Công ty Cổ phần dược phẩm Ampharco U.S.A sản xuất, không đạt yêu cầu chất lượng về chỉ tiêu tính chất (vi phạm mức độ 3).
Bên cạnh đó, Sở này cũng yêu cầu Công ty Cổ phần dược phẩm Ampharco U.S.A và Công ty cổ phần Dadison Hoa Kỳ thực hiện thu hồi triệt để thuốc viên nang mềm SOS Fever® Fort vi phạm nói trên và gửi báo cáo thu hồi, hồ sơ thu hồi về Cục Quản lý Dược, Sở Y tế TP.Hà Nội theo quy định.
Các cơ sở y tế, cơ sở bán buôn, bán lẻ thuốc trên địa bàn khẩn trương rà soát, thu hồi lô thuốc không đạt tiêu chuẩn chất lượng nêu trên. Phòng Y tế các quận, huyện, thị xã thông báo đến các cơ sở hành nghề trên địa bàn quản lý; tiến hành kiểm tra, giám sát việc thực hiện thu hồi của cơ sở (nếu có).
Sở Y tế Hà Nội sẽ kiểm tra, giám sát việc thu hồi của các đơn vị, thông báo để các đơn vị biết, thực hiện và báo cáo việc thực hiện về Sở Y tế.
Trước đó vài ngày Sở Y tế Hà Nội cũng có văn bản thu hồi thuốc Alphatrypa DT không đạt tiêu chuẩn chất lượng. Thuốc do Công ty TNHH Quốc tế Nhật Thành Pharma cung cấp; nơi sản xuất, phân phối là Công ty cổ phần Dược phẩm Trung ương I- Pharbaco do không đạt tiêu chuẩn chất lượng về các chỉ tiêu Định lượng (vi phạm mức độ 2).
Sở Y tế yêu cầu Công ty Cổ phần dược phẩm Trung ương I - Pharbaco và Công ty TNHH Quốc tế Nhật Thành Pharma thực hiện thu hồi triệt để: Thuốc viên nén Alphatrypa DT (Chymotrypsin 4,2mg); SĐT: VN-26281-17; Số lô: 84324; Ngày sản xuất: 25/5/2024; Hạn dùng: 25/5/2026; gửi báo cáo thu hồi, hồ sơ thu hồi theo quy định tại công văn 3288/QLD-CL.
Đồng thời, các cơ sở y tế, cơ sở bán buôn, bán lẻ thuốc trên địa bàn khẩn trương rà soát, thu hồi lô thuốc không đạt tiêu chuẩn chất lượng nêu trên. Phòng Y tế các quận, huyện, thị xã thông báo đến các cơ sở hành nghề trên địa bàn quản lý; tiến hành kiểm tra, giám sát việc thực hiện thu hồi của cơ sở (nếu có).
Được biết thời gian gần đây liên tiếp các loại thuốc vi phạm chất lượng bị thu hồi. Cụ thể, giữa tháng 9/2024, Sở Y tế Hà Nội thông báo thu hồi thuốc Viên nang chứa vi hạt Zovitit (Acyclovir 200mg), số GĐKLH: VN-15819-12, Số lô: 0017, NSX: 03/05/23, HD: 02/05/26 do Công ty S.C. Slavia Pharma S.R.L (Romania) sản xuất, Công ty Cổ phần Dược phẩm Trung ương Codupha nhập khẩu.
Theo đó, Chi nhánh Công ty cổ phần Dược phẩm Trung ương Codupha Hà Nội phối hợp với Công ty cổ phần Dược phẩm Trung ương Codupha tiến hành thu hồi lô thuốc không đạt tiêu chuẩn chất lượng đã phân phối, lập hồ sơ thu hồi, báo cáo việc thu hồi về Sở Y tế Hà Nội (nếu có).
Ngoài loại thuốc nêu trên, Sở Y tế Hà Nội thông báo thu hồi thuốc viên nén Cetecocenzitax (Cinarizin 25mg), Số GĐKLH: VD-20384-13; Số lô: 01/0823; NSX: 030823; HD: 030826 vi phạm mức độ 3 do Công ty cổ phần Dược Trung ương 3 sản xuất.
Sở Y tế Hà Nội yêu cầu các cơ sở y tế công lập trực thuộc ngành, các cơ sở y tế ngoài công lập, các doanh nghiệp kinh doanh thuốc, các cơ sở bán lẻ thuốc trên địa bàn rà soát, thu hồi triệt để lô thuốc nêu trên; gửi báo cáo thu hồi, hồ sơ thu hồi về Sở Y tế, Cục Quản lý Dược theo quy định. Sở Y tế sẽ kiểm tra, giám sát việc thu hồi của các đơn vị, cơ sở.
Phòng Y tế các quận, huyện, thị xã thông báo đến các cơ sở hành nghề trên địa bàn quản lý; tiến hành kiểm tra, giám sát việc thực hiện thu hồi của cơ sở (nếu có).
Lưu ý, phối hợp với các cơ quan truyền thông thông tin tới các cơ sở kinh doanh, sử dụng thuốc và người dân biết để không buôn bán, sử dụng.
Cục Quản lý Dược (Bộ Y tế) cũng có công văn thông báo, thu hồi sản phẩm thuốc viên nén Ubiheal 300 (Thioctic acid 300 mg) của Công ty CP dược phẩm Nam Hà do không đạt tiêu chuẩn chất lượng.
Cục Quản lý Dược yêu cầu Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, Y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc thu hồi lô thuốc Viên nén Ubiheal 300 (Thioctic acid 300 mg) không đạt chất lượng nêu trên.
Bên cạnh đó, công bố thông tin về quyết định thu hồi thuốc trên Trang thông tin điện tử của Sở, kiểm tra và giám sát các đơn vị thực hiện thông báo này; xử lý những đơn vị vi phạm theo quy định hiện hành; báo cáo về Cục Quản lý Dược và cơ quan chức năng có liên quan.
Đồng thời, Cục Quản lý Dược (Bộ Y tế) giao Sở Y tế Hà Nội, Sở Y tế tỉnh Nam Định kiểm tra và giám sát Công ty CP dược phẩm Nam Hà thực hiện việc thu hồi và xử lý thuốc bị thu hồi theo quy định.

-
Tin mới y tế ngày 8/5: Phẫu thuật thành công ca động kinh kháng thuốc nhờ công nghệ ECoG -
Bác sỹ của những "đường mổ vô hình" và giấc mơ y học Việt Nam -
Xuất hiện nhiều hình thức mạo danh MEDLATEC, khách hàng cần cảnh giác -
TP.HCM ghi nhận 4 ca tử vong do bệnh dại, ngành y tế tăng cường giám sát -
Loạt công nghệ điều trị nhãn khoa hiện đại được cập nhật tại Việt Nam -
Nhiều người dân vùng sâu vượt hàng chục km đi tiêm vắc-xin phòng dịch -
Lộ trình khám sức khỏe miễn phí cho toàn dân từ năm 2026
-
 Acecook Việt Nam khởi động dự án trồng 10.500 cây xanh tại tỉnh Quảng Trị - “Gieo mầm hạnh phúc - phủ xanh tương lai”
Acecook Việt Nam khởi động dự án trồng 10.500 cây xanh tại tỉnh Quảng Trị - “Gieo mầm hạnh phúc - phủ xanh tương lai” -
 Giao lưu nhân dân tại Đồng Nai chào mừng 50 năm quan hệ Việt Nam - Thái Lan
Giao lưu nhân dân tại Đồng Nai chào mừng 50 năm quan hệ Việt Nam - Thái Lan -
 CEO Anh Tuấn và Untra Group - Kiến tạo hệ sinh thái ESG cho doanh nghiệp Việt
CEO Anh Tuấn và Untra Group - Kiến tạo hệ sinh thái ESG cho doanh nghiệp Việt -
 Fenica - Căn hộ TOD dành riêng cho giới trẻ chính thức chào sân tại Đông Bắc TP.HCM
Fenica - Căn hộ TOD dành riêng cho giới trẻ chính thức chào sân tại Đông Bắc TP.HCM -
 AMY GRUPO kỷ niệm 10 năm kiến tạo hệ sinh thái vật liệu xây dựng
AMY GRUPO kỷ niệm 10 năm kiến tạo hệ sinh thái vật liệu xây dựng -
SeABank thông báo mời thầu