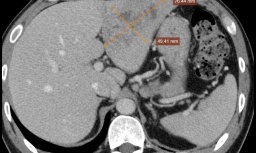
 Bác sỹ cảnh báo nguy cơ áp xe gan từ thói quen ăn rau sống
Bác sỹ cảnh báo nguy cơ áp xe gan từ thói quen ăn rau sống -
 Bác sỹ cảnh báo nguy cơ áp xe gan từ thói quen ăn rau sống
Bác sỹ cảnh báo nguy cơ áp xe gan từ thói quen ăn rau sống -
 Tăng cường năng lực y tế dự phòng cho vùng biển đảo
Tăng cường năng lực y tế dự phòng cho vùng biển đảo -
 Tin mới y tế ngày 17/5: WHO cảnh báo gánh nặng tăng huyết áp toàn cầu ngày càng nghiêm trọng
Tin mới y tế ngày 17/5: WHO cảnh báo gánh nặng tăng huyết áp toàn cầu ngày càng nghiêm trọng -
 Y tế số và cuộc cách mạng dữ liệu đang thay đổi ngành y Việt Nam
Y tế số và cuộc cách mạng dữ liệu đang thay đổi ngành y Việt Nam -
Người Việt tiêu thụ muối gần gấp đôi mức khuyến cáo của Tổ chức Y tế thế giới -
Tin mới y tế ngày 16/5: Xây dựng “bộ khung chuẩn” cho bác sỹ y học cổ truyền
Theo đó, lô thuốc bị thu hồi là viên nén bao phim PymeRoxitil (Roxithromycin 150mg), số giấy đăng ký lưu hành VD-28304-17, số lô: 010522, sản xuất ngày 18/5/2022, hạn dùng 18/5/2025 do Công ty CP Pymepharco sản xuất.
 |
| Ảnh minh hoạ |
Trước đó, ba mẫu thuốc thuộc lô này do Trung tâm Kiểm nghiệm thuốc, mỹ phẩm, thực phẩm tỉnh Đắk Lắk và Viện kiểm nghiệm thuốc TP.HCM thực hiện lấy mẫu, kết quả cho thấy không đạt tiêu chuẩn chất lượng về chỉ tiêu tạp chất liên quan.
Cục Quản lý Dược xác định lô thuốc vi phạm mức độ 2, tức là không bảo đảm đầy đủ hiệu quả điều trị, hoặc có nguy cơ không an toàn cho người sử dụng.
PymeRoxitil là thuốc kháng sinh, được dùng để điều trị viêm họng, viêm amidan, viêm phế quản, viêm xoang, viêm âm đạo, viêm niệu đạo và còn được dùng để điều trị nhiễm khuẩn da và mô mềm, hoặc nhiễm khuẩn răng miệng.
Trước vi phạm của Công ty CP Pymepharco, Cục Quản lý Dược đã yêu cầu đơn vị này phải phối hợp với các nhà phân phối thuốc để thu hồi toàn bộ lô thuốc nói trên trong phạm vi toàn quốc.
Trong thời hạn 2 ngày kể từ ngày ra thông báo, công ty này phải gửi thông báo thu hồi tới các cơ sở bán buôn, bán lẻ, sử dụng sản phẩm.
Công ty CP Pymepharco phải gửi báo cáo thu hồi về Cục Quản lý Dược trong vòng 18 ngày kể từ ngày ra thông báo.
Cục Quản lý dược cũng yêu cầu doanh nghiệp báo cáo phải nêu rõ số lượng sản xuất, số lượng phân phối, ngày sản xuất, số lượng thu hồi và bằng chứng về việc thực hiện thu hồi tại các cơ sở bán buôn, bán lẻ, sử dụng lô thuốc PymeRoxitil trên.
Với Sở Y tế các tỉnh, thành phố; y tế các ngành Cục Quản lý dược yêu cầu thông báo cho các cơ sở kinh doanh, sử dụng sản phẩm thu hồi, kiểm tra và giám sát các đơn vị thực hiện thông báo này.
Riêng Sở Y tế Đắk Lắk và Phú Yên được giao kiểm tra và giám sát Công ty CP Pymepharco thực hiện việc thu hồi và xử lý thuốc bị thu hồi theo quy định.
Cục Quản lý Dược, Bộ Y tế, ký văn bản yêu cầu thu hồi toàn quốc thuốc viên nang cứng H-inzole, số giấy đăng ký lưu hành VN18555-14, số lô: HT4-51 vì vi phạm chất lượng mức độ 3.
Lô thuốc viên nang cứng H-inzole, số giấy đăng ký lưu hành VN18555-14, số lô: HT4-51 được sản xuất ngày 18-10-2022, hạn dùng 17-10-2024 do Công ty Lark Laboratories (India) Ltd India sản xuất, Công ty cổ phần Dược phẩm Hà Tây nhập khẩu.
ý do thu hồi được đưa ra là nhà chức trách xác định lô thuốc nêu trên vi phạm chất lượng mức độ 3 (vi phạm mức độ 3 là thuốc vi phạm chất lượng, về cảm quan: biến đổi màu sắc; chênh lệch khối lượng của thuốc viên; hàm lượng không đạt...).
Thuốc chữa bệnh là loại hàng hóa đặc biệt vì liên quan đến sức khỏe và tính mạng con người. Dù vậy, thời gian gần đây tình trạng thuốc kém chất lượng lọt ra thị trường vẫn luôn diễn ra khiến người dân hết sức lo lắng.
Nguy hiểm khi dùng thuốc kém chất lượng là vấn đề ai cũng biết, song theo thừa nhận của các cơ quan quản lý, phải mất rất nhiều thời gian để cơ quan chức năng đưa ra được kết luận một sản phẩm thuốc kém chất lượng. Vậy nên, với người dân, để biết sản phẩm nào tốt, sản phẩm nào không tốt khó như việc hái sao trên trời.
Để phát hiện thuốc kém chất lượng, chỉ có cách duy nhất là đưa đến kiểm nghiệm tại Viện Kiểm nghiệm thuốc Trung ương. Tuy vậy, có những loại thuốc, mất rất nhiều thời gian kiểm nghiệm, đến khi có kết quả thì thuốc đã nằm trong cơ thể người bệnh.
Lý giải nguyên nhân của tình trạng trên, theo các chuyên gia, việc ra các quyết định thu hồi, cảnh báo chất lượng, tương tác hay tai biến thuốc ở Việt Nam thường chậm hàng tháng, thậm chí nhiều tháng so với cảnh báo của cơ quan quản lý dược châu Âu và Mỹ.
Bên cạnh đó, để thuốc kém chất lượng có cơ hội tiếp cận với người dùng là do sự minh bạch thông tin và giám sát việc đấu thầu các gói thầu cung cấp thuốc còn nhiều bất cập.
Nhìn ra thế giới, có thể thấy, đa số các nước rất chú trọng việc xây dựng hàng rào kỹ thuật thuốc nhập khẩu; nghiên cứu giới hạn số lượng nhập khẩu theo nhu cầu, nhất là những mặt hàng đã sản xuất trong nước.
Điểm mạnh ở các nước là tiến hành kiểm tra định kỳ nhà máy sản xuất, kiểm nghiệm sản phẩm mà chi phí do bên xuất khẩu chi trả. Khi kiểm tra đủ điều kiện mới cho nhập thuốc.
Trong khi đó, Việt Nam chưa có chiến lược định hướng rõ ràng về thuốc cần ưu tiên hoặc hạn chế nhập khẩu, nên chưa có các giải pháp cụ thể.

-
Y tế số và cuộc cách mạng dữ liệu đang thay đổi ngành y Việt Nam -
Người Việt tiêu thụ muối gần gấp đôi mức khuyến cáo của Tổ chức Y tế thế giới -
Tin mới y tế ngày 16/5: Xây dựng “bộ khung chuẩn” cho bác sỹ y học cổ truyền -
TP.HCM hỗ trợ toàn diện Bệnh viện Bà Rịa, hướng tới bệnh viện cửa ngõ phía Đông Nam -
Tuần Lễ Vàng 2026 - Tiếp thêm hy vọng cho các gia đình hiếm muộn -
Dịch sốt xuất huyết tăng cao, chuyên gia cảnh báo biến chứng nặng của bệnh -
Tin mới y tế ngày 15/5: Giảm nguy cơ lây bệnh lao trong cộng đồng
-
 EVF công bố bổ nhiệm nhân sự cấp cao
EVF công bố bổ nhiệm nhân sự cấp cao -
 Hoàng Thu Hiền: Kinh doanh món ăn gia đình bằng sự tử tế và cái tâm của người làm mẹ
Hoàng Thu Hiền: Kinh doanh món ăn gia đình bằng sự tử tế và cái tâm của người làm mẹ -
 Điều hòa Daikin FTKM cho phép tùy chỉnh độ ẩm theo nhu cầu
Điều hòa Daikin FTKM cho phép tùy chỉnh độ ẩm theo nhu cầu -
 Công bố Top 10 doanh nghiệp đổi mới sáng tạo và kinh doanh hiệu quả 2026 ngành Logistics
Công bố Top 10 doanh nghiệp đổi mới sáng tạo và kinh doanh hiệu quả 2026 ngành Logistics -
 Công bố Top 10 doanh nghiệp đổi mới sáng tạo và kinh doanh hiệu quả 2026 ngành Dược - Thiết bị y tế
Công bố Top 10 doanh nghiệp đổi mới sáng tạo và kinh doanh hiệu quả 2026 ngành Dược - Thiết bị y tế -
 Hạ tầng bứt tốc cùng vốn FDI đổ về: Đồng Nai vươn mình thành cực tăng trưởng mới
Hạ tầng bứt tốc cùng vốn FDI đổ về: Đồng Nai vươn mình thành cực tăng trưởng mới