 Nhiều người dân vùng sâu vượt hàng chục km đi tiêm vắc-xin phòng dịch
Nhiều người dân vùng sâu vượt hàng chục km đi tiêm vắc-xin phòng dịch -
 Nhiều người dân vùng sâu vượt hàng chục km đi tiêm vắc-xin phòng dịch
Nhiều người dân vùng sâu vượt hàng chục km đi tiêm vắc-xin phòng dịch -
 Lộ trình khám sức khỏe miễn phí cho toàn dân từ năm 2026
Lộ trình khám sức khỏe miễn phí cho toàn dân từ năm 2026 -
 Tin mới y tế ngày 7/5: Quy định mới về xử phạt sai phạm trong lĩnh vực y tế
Tin mới y tế ngày 7/5: Quy định mới về xử phạt sai phạm trong lĩnh vực y tế -
 Phế cầu khuẩn gây ra hơn 1.6 triệu ca tử vong trên toàn cầu
Phế cầu khuẩn gây ra hơn 1.6 triệu ca tử vong trên toàn cầu -
Thuốc giá rẻ không còn chiếm ưu thế tuyệt đối trong đấu thầu -
Vắc-xin được kỳ vọng giảm nguy cơ các ca bệnh nặng do sốt xuất huyết
Đây là loại thuốc có tác dụng giảm đau, hạ sốt (thành phần chính là paracetamol và cafein) chỉ dùng theo đơn của bác sĩ.
 |
| Cục Quản lý dược, Bộ Y tế có Công văn số 5673/QLD-CL gửi sở y tế các tỉnh, thành phố trực thuộc Trung ương về mẫu thuốc Ophazidon giả. |
Cục Quản lý dược đề nghị, sở y tế các tỉnh, thành phố phối hợp với các cơ quan truyền thông, thông tin tới các cơ sở buôn bán, sử dụng thuốc và người dân biết để không buôn bán, sử dụng sản phẩm Ophazidon giả có các dấu hiệu nhận biết nêu trên.
Bên cạnh đó, Cục Quản lý dược cũng đề nghị các cơ quan chức năng liên quan kiểm tra các cơ sở kinh doanh thuốc trên địa bàn; xác minh thông tin và truy tìm nguồn gốc về sản phẩm Ophazidon giả nêu trên.
Đồng thời, các cơ quan chức năng xử lý các tổ chức, cá nhân vi phạm theo quy định hiện hành; kịp thời phát hiện và ngăn chặn việc sản xuất, buôn bán và sử dụng thuốc Ophazidon giả.
Trên thị trường, thuốc Ophazidon là thuốc giảm đau có thành phần chính: Paracetamol, cafein. Thuốc có chỉ định với các trường hợp đau nửa đầu, nhức đầu, đau nhức toàn thân, viêm họng, viêm xoang, đau bụng kinh, sốt, viêm, đau răng… Thuốc do Công ty cổ phần Dược phẩm Hà Nội sản xuất, đóng gói lọ gồm 100 viên nén.
Trước đó, Trung tâm Kiểm nghiệm dược phẩm, mỹ phẩm tỉnh Cao Bằng tiến hành lấy mẫu xác định chất lượng của sản phẩm trên nhãn ghi: Viên nén Ophazidon; số đăng ký: VD-26803-17; số lô: 480821; ngày sản xuất: 17/8/2021; hạn sử dụng: 17/8/2023, Công ty cổ phần Dược phẩm Hà Nội.
Kết quả kiểm nghiệm, mẫu sản phẩm này không đạt tiêu chuẩn chất lượng về các chỉ tiêu định tính, định lượng (cafein) và định lượng (paracetamol). Sau khi xác minh, mẫu thuốc không đạt chất lượng này được xác định sản phẩm giả mạo.
Để bảo đảm an toàn cho người sử dụng, Cục Quản lý dược đề nghị, sở y tế các tỉnh, thành phố trực thuộc trung ương, y tế các ngành thông báo cho các cơ sở kinh doanh, sử dụng thuốc thông tin về thuốc giả trên nhãn ghi: Viên nén Ophazidon; số đăng ký: VD-26803-17; số lô: 480821; ngày sản xuất: 17/8/2021; hạn sử dụng: 17/8/2023, Công ty cổ phần Dược phẩm Hà Nội có các đặc điểm, dấu hiệu phân biệt với thuốc thật.
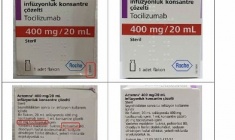
Cách đây chưa lâu, Cục Quản lý Dược, Bộ Y tế cảnh báo thuốc Actemra 400 mg/20 mL chưa cấp phép nhập khẩu, chưa cấp giấy đăng ký lưu hành tại Việt Nam, nhưng trên thị trường phát hiện mẫu sản phẩm nghi ngờ là thuốc giả, trên nhãn ghi: Actemra 400 mg/20 mL, số lô B2101B32.
Một loại thuốc khác là Stivarga 40mg và Xarelto 10mg/15mg/20mg cũng bị nghi ngờ là thuốc giả. Đây là các thuốc có chỉ định điều trị ung thư và đông máu.
Mẫu các sản phẩm nghi ngờ là thuốc giả do Công ty Luật TNHH T&G phát hiện được bán trên thị trường và một số website (https://healthyungthu.com, https://nhathuoclp.com, https://thuocdactrigan.com).
-
Thuốc giá rẻ không còn chiếm ưu thế tuyệt đối trong đấu thầu -
Vắc-xin được kỳ vọng giảm nguy cơ các ca bệnh nặng do sốt xuất huyết -
Công nghệ y tế thông minh nổi bật tại Vietnam Medi - Pharm 2026 -
Tin mới y tế ngày 6/5: Phẫu thuật nội soi 3D cứu hai ca ung thư thực quản phức tạp -
MEDLATEC miễn phí bộ 3 xét nghiệm đánh giá mức độ hủy hoại tế bào gan, giảm 50% siêu âm đàn hồi mô gan -
Bộ Y tế cảnh báo khẩn vi rút Hanta lây truyền từ chuột -
Góc hàm sưng to phát hiện u tuyến nước bọt hiếm gặp
-
 Kinh tế tư nhân trong kỷ nguyên vươn mình: EVF tinh gọn, tinh nhuệ hóa bộ máy để phát triển bền vững
Kinh tế tư nhân trong kỷ nguyên vươn mình: EVF tinh gọn, tinh nhuệ hóa bộ máy để phát triển bền vững -
 Agribank được Moody’s Ratings điều chỉnh triển vọng xếp hạng từ “Ổn định” lên “Tích cực”
Agribank được Moody’s Ratings điều chỉnh triển vọng xếp hạng từ “Ổn định” lên “Tích cực” -
 Củng cố vai trò cầu nối, Hiệp hội Bất động sản Hải Phòng bước vào giai đoạn mới
Củng cố vai trò cầu nối, Hiệp hội Bất động sản Hải Phòng bước vào giai đoạn mới -
 Masan Group ước lãi 4.600 tỷ đồng trong nửa đầu năm 2026, MSR góp phần giảm nợ vay
Masan Group ước lãi 4.600 tỷ đồng trong nửa đầu năm 2026, MSR góp phần giảm nợ vay -
 Nutifood tài trợ 9,3 tỷ đồng cho đội Bóng chuyền nữ TP.HCM, tiếp sức trở lại đỉnh cao
Nutifood tài trợ 9,3 tỷ đồng cho đội Bóng chuyền nữ TP.HCM, tiếp sức trở lại đỉnh cao -
 Cập nhật giá đơn vị Quỹ liên kết đơn vị của AIA Việt Nam ngày 6/5/2026
Cập nhật giá đơn vị Quỹ liên kết đơn vị của AIA Việt Nam ngày 6/5/2026














