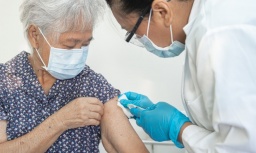
 Dấu hiệu dễ nhầm với zona thần kinh khiến nhiều người xử trí sai
Dấu hiệu dễ nhầm với zona thần kinh khiến nhiều người xử trí sai -
 Dấu hiệu dễ nhầm với zona thần kinh khiến nhiều người xử trí sai
Dấu hiệu dễ nhầm với zona thần kinh khiến nhiều người xử trí sai -
 Thúc đẩy ứng dụng AI trong bảo hiểm y tế và chăm sóc sức khỏe
Thúc đẩy ứng dụng AI trong bảo hiểm y tế và chăm sóc sức khỏe -
 Gia tăng mạo danh dịch vụ xét nghiệm tại nhà: Hệ thống Y tế MEDLATEC đưa ra khuyến cáo xác minh
Gia tăng mạo danh dịch vụ xét nghiệm tại nhà: Hệ thống Y tế MEDLATEC đưa ra khuyến cáo xác minh -
 Viêm não Nhật Bản: Trả giá đắt vì quên tiêm nhắc lại
Viêm não Nhật Bản: Trả giá đắt vì quên tiêm nhắc lại -
Tin mới y tế ngày 10/6: Y học sơ sinh viết tiếp sự sống cho bé gái sinh non 29 tuần -
Tôn vinh những người viết tiếp sự sống bằng giọt máu hồng
Theo đề cương nghiên cứu, thử nghiệm lâm sàng giai đoạn 2 vắc-xin Nano Covax kéo dài đến tháng 2/2022. Tuy nhiên, nhằm đẩy nhanh tiến độ phát triển vắc-xin, Hội đồng đạo đức quốc gia đã họp khẩn cấp để đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 2 và cho phép thực hiện thử nghiệm lâm sàng giai đoạn 3.
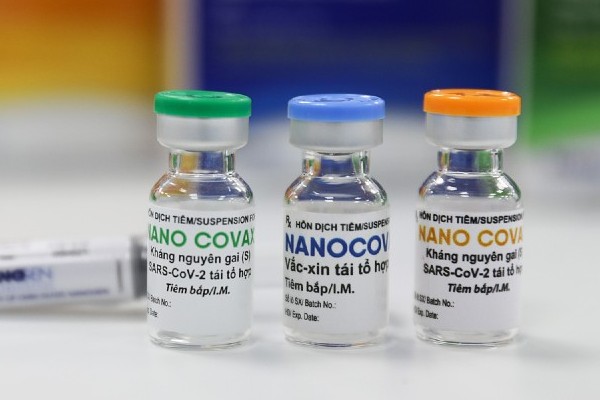 |
| Ảnh minh họa. |
Đối với thử nghiệm lâm sàng giai đoạn 3, để sớm có kết quả về tính sinh miễn dịch Hội đồng cho phép chỉ thực hiện các xét nghiệm về tính sinh miễn dịch ở giai đoạn 3a trên 1.000 người tình nguyện.
Cho đến ngày 6/8/2021, Hội đồng đạo đức quốc gia chưa nhận được hồ sơ, báo cáo chính thức nào từ các nghiên cứu viên chính và Tổ chức nhận thử về hiệu lực bảo vệ của vắc-xin Nanogen.
Kết quả cuộc họp sáng ngày 7/8/2021, Hội đồng đã thống nhất nghiệm thu kết quả thử nghiệm lâm sàng giai đoạn 1 vắc-xin Nanocovax với dữ liệu theo dõi đến tháng thứ 6 kể từ liều tiêm đầu tiên của giai đoạn 1 trên 60 người tình nguyện với 3 mức liều 25 mcg, 50 mcg, 75 mcg.
Trên cơ sở cập nhật kết quả đánh giá giữa kỳ giai đoạn 2 đến thời điểm hiện tại, Hội đồng quyết định tiếp tục cho phép triển khai thử nghiệm lâm sàng giai đoạn 3 với mức liều 25mcg theo đề cương nghiên cứu đã được phê duyệt.
Tại cuộc họp, Thứ trưởng Bộ Y tế Trần Văn Thuấn khẳng định, đối với việc nghiên cứu phát triển vắc-xin phòng chống Covid-19 trong nước, chúng ta khẩn trương nhưng cần phải khoa học, chặt chẽ để đảm bảo số liệu đưa ra đủ tin cậy.
Theo Thứ trưởng Bộ Y tế, ông đồng tình với ý kiến của Chủ tịch Hội đồng về việc cần thành lập ngay tổ hỗ trợ, phân tích, đánh giá, giám sát số liệu và quy trình của 2 đơn vị tham gia nghiên cứu thử nghiệm lâm sàng, và phải có báo cáo trước ngày 14/8/2021.
Lãnh đạo Bộ Y tế cũng đề nghị các đơn vị nhận thử như Học viện Quân y, Viện Pasteur TP.HCM và đơn vị độc lập là Viện Vệ sinh dịch tễ Trung ương kết hợp với nhà sản xuất là Công ty Cổ phần Công nghệ sinh học dược Nanogen: Sau khi Hội đồng đã cho phép nghiệm thu kết quả giai đoạn 1 và giữa kỳ giai đoạn 2 phải khẩn trương hoàn thiện.
Thứ trưởng đề nghị Hội đồng tiếp tục họp vào ngày 15/8/2021 để đánh giá kết quả giai đoạn 3a.
Lãnh đạo Bộ Y tế đề nghị cân nhắc xem xét có tiến hành thêm nghiên cứu bổ sung về việc tiêm mũi 3 vắc-xin Nanocovax hay không. Bên cạnh đó, xem xét bổ sung các chủng mới của virus Corona (như chủng Delta) vào nghiên cứu ở thời điểm thích hợp.
Đặc biệt, theo yêu cầu của Thứ trưởng Bộ Y tế, quan điểm của Bộ Y tế rất ủng hộ, tạo mọi điều kiện để các tỉnh tham gia thử nghiệm lâm sàng. Tuy nhiên, phải tuân thủ đúng theo các quy trình, quy định về thử nghiệm lâm sàng. Bộ Y tế không đồng ý việc lợi dụng ưu tiên thử nghiệm lâm sàng vào mục đích thương mại.
Được biết, hiện tại, Khánh Hoà và Bình Dương là 2 địa phương đầu tiên xin tham gia thử nghiệm vắc-xin Nanocovax số lượng lớn.
Trong đó Bình Dương xin tiêm thử nghiệm Nanocovax cho 200.000 công nhân, người lao động tại các doanh nghiệp, chiếm khoảng 16% trong tổng số hơn 1,2 triệu người lao động tại các nhà máy, xí nghiệp trong tỉnh.
Lý do Bình Dương đưa ra là tình hình dịch tại tỉnh đang diễn biến phức tạp, số ca mắc đã vượt 18.000 ca và những ngày tới sẽ tiếp tục tăng trong khi lượng vắc xin phân bổ chưa nhiều.
UBND tỉnh Khánh Hòa cũng đề nghị Bộ Y tế sớm cho phép tiêm thí điểm vắc xin Covid-19 Nanocovax trên địa bàn tỉnh để góp phần đưa Nanocovax sớm đến tay người dân. Ngoài ra, Đồng Tháp cũng đã có văn bản chỉ đạo, mong muốn được tham gia thử nghiệm.

-
Tin mới y tế ngày 10/6: Y học sơ sinh viết tiếp sự sống cho bé gái sinh non 29 tuần -
Tôn vinh những người viết tiếp sự sống bằng giọt máu hồng -
Quảng Ninh: Chi hơn 183 tỷ đồng chăm lo cho trẻ em -
Siết chặt quản lý thực phẩm giả, ngăn quảng cáo thổi phồng trên môi trường mạng -
Bệnh truyền nhiễm: Mối đe dọa không biên giới và bài toán ứng phó trong kỷ nguyên mới -
Bác sỹ cảnh báo khối u nhỏ ở bàn tay không nên chủ quan -
Tin mới y tế ngày 9/6: Thúc đẩy bệnh viện thông minh bằng trí tuệ nhân tạo
-
 “Con đường tương lai” của nhà văn Nguyễn Xuân Tuấn được giới thiệu tới bạn bè quốc tế tại Diễn đàn Tương lai ASEAN 2026
“Con đường tương lai” của nhà văn Nguyễn Xuân Tuấn được giới thiệu tới bạn bè quốc tế tại Diễn đàn Tương lai ASEAN 2026 -
 Samsung đẩy mạnh hợp tác toàn diện với các trường đại học trong lĩnh vực kỹ thuật và công nghệ tại Việt Nam
Samsung đẩy mạnh hợp tác toàn diện với các trường đại học trong lĩnh vực kỹ thuật và công nghệ tại Việt Nam -
 Manulife phát triển đội ngũ tư vấn tài chính - bảo hiểm thế hệ mới
Manulife phát triển đội ngũ tư vấn tài chính - bảo hiểm thế hệ mới -
Sức hút từ hệ sinh thái VPBank tại Ngày Tài chính số 2026
-
 Đoàn công tác tỉnh Phú Thọ làm việc với Đại sứ quán Việt Nam tại Phần Lan
Đoàn công tác tỉnh Phú Thọ làm việc với Đại sứ quán Việt Nam tại Phần Lan -
 Phát huy hiệu quả các dự án, công trình môi trường
Phát huy hiệu quả các dự án, công trình môi trường