 “Ðại phẫu” trong cắt giảm thủ tục hành chính lĩnh vực y tế
“Ðại phẫu” trong cắt giảm thủ tục hành chính lĩnh vực y tế -
 “Ðại phẫu” trong cắt giảm thủ tục hành chính lĩnh vực y tế
“Ðại phẫu” trong cắt giảm thủ tục hành chính lĩnh vực y tế -
 Bộ Y tế chỉ đạo khẩn ứng phó Ebola, yêu cầu bệnh viện sẵn sàng cách ly
Bộ Y tế chỉ đạo khẩn ứng phó Ebola, yêu cầu bệnh viện sẵn sàng cách ly -
 Phát động chiến dịch bảo vệ thanh thiếu niên trước làn sóng thuốc lá điện tử
Phát động chiến dịch bảo vệ thanh thiếu niên trước làn sóng thuốc lá điện tử -
 Trục lợi quỹ bảo hiểm y tế sẽ bị xử lý nghiêm theo quy định mới
Trục lợi quỹ bảo hiểm y tế sẽ bị xử lý nghiêm theo quy định mới -
Tin mới y tế ngày 24/5: Suy tim vì lạm dụng thuốc giảm đau -
WHO đánh giá nguy cơ Ebola xâm nhập Việt Nam
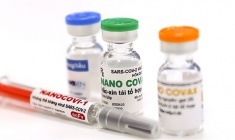
Ngày 18/9, Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia (Hội đồng Đạo đức) đã họp khẩn cấp để đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 của vắc-xin Nano Covax với kết quả nghiên cứu tính đến ngày 2/9.
Đại diện Hội đồng Đạo đức cho biết, trên cơ sở xem xét hồ sơ, kết quả nghiên cứu và ý kiến của các thành viên tham dự họp, hội đồng đã thống nhất về việc sử dụng các kết quả nghiên cứu thử nghiệm lâm sàng tính đến thời điểm đánh giá kết quả giữa kỳ giai đoạn 3, gửi cho Thường trực Hội đồng Tư vấn cấp giấy đăng ký thuốc, nguyên liệu làm thuốc để xem xét cấp giấy đăng ký lưu hành có điều kiện vắc-xin Nano Covax theo quy định.
GS.TS Trương Việt Dũng, Chủ tịch Hội đồng đạo đức cho hay, Nano Covax của Công ty Nanogen đạt các yêu cầu về an toàn và tính sinh miễn dịch.
Trước đó, ngày 29/8, Hội đồng tư vấn cấp Giấy đăng ký lưu hành thuốc và nguyên liệu làm thuốc đã họp để nghe báo và xem xét việc cấp phép khẩn cấp cho vắc-xin Nano Covax.
 |
| Hội đồng Đạo đức đồng ý chuyển hồ sơ Nano Covax sang hội đồng cấp giấy đăng ký lưu hành. |
Vắc-xin Nano Covax phát triển bằng công nghệ tái tổ hợp protein, một công nghệ khá mới so với mặt bằng sản xuất vắc-xin ở Việt Nam. Ở giai đoạn ban đầu, tháng 4/2020, dự án này không phải là dự án có tiến độ phát triển tốt nhất.
Nhưng sau đó "cuộc đua" vắc-xin nóng lên, tiến độ vắc-xin nhanh dần. Tháng 7 và 8/2020 đã có 2 đơn vị gửi mẫu thử vắc-xin trên động vật đi đánh giá ở nước ngoài là Covivac và Nano Covax.
Cuối năm 2020, Bộ Y tế cho phép Nano Covax triển khai thử nghiệm trên người. Ngày 17/12/2020 bắt đầu đợt tiêm thử nghiệm đầu tiên với 3 người tình nguyện (2 người sinh năm 2000, đang cùng là sinh viên, và 1 nữ giáo viên sinh năm 1980) được chọn tiêm thử nghiệm đầu tiên, tại Học viện Quân y.
Cuối tháng 2/2021, Nano Covax được chuyển sang giai đoạn 2 thử nghiệm trên người và đầu tháng 6 chuyển sang giai đoạn 3.
Từ ngày 17/12/2020 - 7/2/2021, Học viện Quân y tiêm thử nghiệm lâm sàng giai đoạn 1 vắc-xin Nanocovax trên 60 tình nguyện viên với 3 nhóm liều 25mcg, 50mcg và 75mcg để đánh giá tính an toàn.
Kết quả, vắc-xin có độ an toàn đạt 100%, hiệu quả bảo vệ người tiêm không bị nhiễm virus SARS-CoV-2 lên đến 90% và tất cả đều sinh miễn dịch tốt.
Đến ngày 26/2/2021, Nanocovax bắt đầu thử nghiệm lâm sàng giai đoạn 2 với 554 tình nguyện viên tham gia.
Kết quả, vắc-xin an toàn, 100% tình nguyện viên đều sinh miễn dịch. Đặc biệt tỉ lệ chuyển đổi huyết thanh của Nanocovax đạt đến 99,4% và kháng thể sinh ra có thể chống lại chủng Vũ Hán, Anh, Nam Phi.
Các phản ứng phụ của Nanocovax thậm chí còn thấp hơn nhiều loại vắc-xin hàng đầu thế giới đang được sử dụng hiện nay và chưa ghi nhận trường hợp nào sốc phản vệ. Do đó Hội đồng Đạo đức, Bộ Y tế quyết định chọn duy nhất nhóm liều 25mcg cho nghiên cứu giai đoạn 3.
Ngày 11/6, Bộ Y tế chính thức phê duyệt đề cương thử nghiệm giai đoạn 3 vắc-xin Nanocovax trên quy mô 13.000 người, trong đó giai đoạn 3a tiêm 1.000 người, giai đoạn 3b tiêm 12.000 còn lại. Đây là giai đoạn quan trọng nhất để đánh giá hiệu quả, độ an toàn của vắc-xin.
Ban đầu, Bộ Y tế dự định triển khai thử nghiệm pha 3a, khi có kết quả sẽ đánh giá trước khi tiêm giai đoạn 3b.
Tuy nhiên sau khi có ý kiến chỉ đạo của Thủ tướng, ngày 25/6, Hội đồng Đạo đức đã đồng ý đẩy nhanh tiến độ thử nghiệm, tiêm luôn vắc-xin cho 12.000 tình nguyện viên còn lại. Bộ Y tế cho biết, dù đẩy nhanh nhưng không bỏ sót giai đoạn, ưu tiên cao nhất việc đảm bảo an toàn và chính xác trong nghiên cứu.
Ngày 22/6, Công ty Nanogen có văn bản gửi Thủ tướng Chính phủ mong muốn vắc-xin Nano Covax sớm được cấp phép khẩn, tương tự các loại của Nga, Trung Quốc và Ấn Độ.
Theo vị lãnh đạo của đơn vị này, vắc-xin Nano Covax đã chứng minh được những thành công bước đầu, Hội đồng đạo đức trong nghiên cứu y sinh chấp thuận và đánh giá tốt, kết quả thử nghiệm lâm sàng, khả năng sinh miễn dịch của vắc-xin Nano Covax đạt 99,4%.
Tuy nhiên, ông Nguyễn Ngô Quang, Phó cục trưởng Cục Khoa học công nghệ và Đào tạo, Bộ Y tế, cho rằng đây chỉ mới là tính sinh miễn dịch. Miễn dịch này có giảm được tỷ lệ mắc Covid-19 hoặc giảm nhẹ tình trạng bệnh hay không chưa có kết quả.
Theo ông Quang, loại vắc-xin này đang còn trong quá trình nghiên cứu, thử nghiệm và chưa có dữ liệu. Kiến nghị từ Công ty Nanogen lên Thủ tướng Chính phủ rất khó được chấp thuận bởi đây thuộc thẩm quyền chuyên môn của Bộ Y tế. Để quyết định có cấp phép khẩn cấp hay không, cơ quan này cần có các dữ liệu khoa học.
Ngày 25/6, Bộ Y tế, Hội đồng Đạo đức quốc gia tổ chức họp khẩn với các đơn vị liên quan đánh giá tiến độ thử nghiệm và kế hoạch mở rộng địa điểm thử nghiệm vắc-xin Nano Covax của Công ty Nanogen.
Hội đồng Đạo đức quốc gia đánh giá vắc-xin Nano Covax an toàn, bước đầu có tính sinh miễn dịch. Tuy nhiên, để đánh giá hiệu lực bảo vệ cần thêm thời gian và số lượng mẫu nghiên cứu, đặc biệt cần có thêm kết quả đánh giá trong phòng thí nghiệm.
Ngày 7/8, Hội đồng Đạo đức trong nghiên cứu y sinh học Quốc gia đã họp khẩn cấp để nghiệm thu kết quả thử nghiệm lâm sàng giai đoạn 1, đánh giá kết quả giữa kỳ thử nghiệm giai đoạn 2.
Ngày 28/8, thông tin chính thức từ Bộ Y tế cho biết, Hội đồng Đạo đức quốc gia thống nhất sử dụng các kết quả nghiên cứu thử nghiệm lâm sàng tính đến thời điểm đánh giá kết quả giữa kỳ giai đoạn 3a vắc-xin Nano Covax gửi cho Thường trực Hội đồng Tư vấn cấp giấy đăng ký thuốc, nguyên liệu làm thuốc để xem xét cấp giấy đăng ký lưu hành có điều kiện vắc-xin Nanocovax theo quy định.
Trong trường hợp vắc-xin Nanocovax được cấp giấy đăng ký lưu hành, vắc-xin Nanocovax có thể chỉ được sử dụng có điều kiện theo số lượng và kế hoạch được Bộ Y tế phê duyệt, những người sử dụng vắc-xin này cần được theo dõi chặt chẽ về tính an toàn tương tự như với đối tượng nghiên cứu giai đoạn 3b.
Ngày 29/8, Hội đồng tư vấn cấp Giấy đăng ký lưu hành thuốc và nguyên liệu làm thuốc đã họp để nghe báo và xem xét việc cấp phép khẩn cấp cho vắc-xin Nano Covax. Tuy nhiên tại cuộc họp chưa có quyết định nào được đưa ra, Hội đồng vẫn yêu cầu Nonogen bổ sung một số thông tin liên quan về vắc-xin Nano Covax.
-
Tin mới y tế ngày 24/5: Suy tim vì lạm dụng thuốc giảm đau -
WHO đánh giá nguy cơ Ebola xâm nhập Việt Nam -
MEDLATEC chẩn đoán sớm, điều trị thành công bệnh nhân nhiễm khuẩn huyết nặng trên nền đái tháo đường type 2 -
Hiểu đúng về vắc-xin HPV để bảo vệ trước nguy cơ ung thư -
Mở “luồng xanh” phát triển doanh nghiệp y tế công nghệ cao -
Tin mới y tế ngày 23/5: Nhiều bệnh lý của mắt nguy hiểm bị phát hiện muộn, nguy cơ mù lòa gia tăng -
Y học tái tạo bước vào giai đoạn bùng nổ, bệnh viện Việt Nam tăng tốc hội nhập quốc tế
-
 Samsung tiếp tục tuyển dụng kỹ sư, cử nhân và thực tập sinh cho các nhà máy ở Việt Nam
Samsung tiếp tục tuyển dụng kỹ sư, cử nhân và thực tập sinh cho các nhà máy ở Việt Nam -
Hệ thống Trường quốc tế Hoa Kỳ APU ghi dấu ấn với 30 triệu USD học bổng cho học sinh tốt nghiệp năm 2026
-
 Vinacomin và Tập đoàn Marubeni (Nhật Bản): Thúc đẩy hợp tác toàn diện và bền vững
Vinacomin và Tập đoàn Marubeni (Nhật Bản): Thúc đẩy hợp tác toàn diện và bền vững -
 Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành Vật liệu xây dựng
Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành Vật liệu xây dựng -
 Nhơn Trạch 3 và Nhơn Trạch 4: Dấu ấn nổi bật của PV Power năm 2025
Nhơn Trạch 3 và Nhơn Trạch 4: Dấu ấn nổi bật của PV Power năm 2025 -
 Cơ hội trúng 500 triệu đồng khi gửi tiền dự thưởng trên Agribank Plus
Cơ hội trúng 500 triệu đồng khi gửi tiền dự thưởng trên Agribank Plus














