 Bộ Y tế siết chặt quy định cấm khói thuốc lá tại bệnh viện
Bộ Y tế siết chặt quy định cấm khói thuốc lá tại bệnh viện -
 Bộ Y tế siết chặt quy định cấm khói thuốc lá tại bệnh viện
Bộ Y tế siết chặt quy định cấm khói thuốc lá tại bệnh viện -
 TP.HCM siết giám sát cửa khẩu, chủ động ngăn nguy cơ dịch Ebola xâm nhập
TP.HCM siết giám sát cửa khẩu, chủ động ngăn nguy cơ dịch Ebola xâm nhập -
 Bộ Y tế thúc đẩy bệnh án điện tử, mở rộng nền tảng chăm sóc sức khỏe số
Bộ Y tế thúc đẩy bệnh án điện tử, mở rộng nền tảng chăm sóc sức khỏe số -
 Nâng hiệu quả quản lý an toàn thực phẩm từ hành động thực chất ở cơ sở
Nâng hiệu quả quản lý an toàn thực phẩm từ hành động thực chất ở cơ sở -
Sốt xuất huyết tăng, TP.HCM và Hà Nội kích hoạt cao điểm chống dịch -
Tin mới y tế ngày 19/5: Mạng xã hội sẽ trở thành nguồn giám sát dịch bệnh truyền nhiễm
Thứ trưởng Bộ Y tế giao Cục Y tế dự phòng làm đầu mối tham mưu về việc hướng dẫn tiêm vắc-xin Covid-19 mũi nhắc lại, vừa triển khai vừa theo dõi kinh nghiệm của các quốc gia khác.
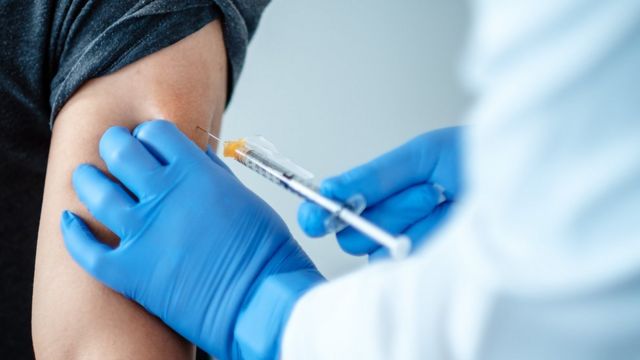 |
| Thứ trưởng Bộ Y tế Trần Văn Thuấn đề nghị Cục Quản lý Dược xây dựng đề cương nghiên cứu thử nghiệm lâm sàng liều nhắc lại vắc-xin nội trước 30/3. |
Ngoài ra, Cục Quản lý Dược làm đầu mối xây dựng, ban hành hướng dẫn tiêu chí cấp phép vắc-xin Covid-19 sản xuất trong nước với chỉ định cho liều nhắc lại, hoàn thành trước ngày 30/3.
Bộ cũng yêu cầu Cục Khoa học công nghệ và Đào tạo hướng dẫn xây dựng đề cương nghiên cứu thử nghiệm lâm sàng liều nhắc lại với vắc-xin Covid-19 sản xuất trong nước; theo dõi, đôn đốc, báo cáo những bất cập, khó khăn khi thử nghiệm lâm sàng.
Thứ trưởng Bộ Y tế cũng đề nghị các đơn vị bố trí đủ nhân lực, tăng cường các biện pháp bảo đảm an toàn tuyệt đối cho người tình nguyện tham gia nghiên cứu, bảo đảm chất lượng dữ liệu nghiên cứu trong suốt thời gian nghiên cứu theo đề cương đã được Bộ Y tế phê duyệt.
Đặc biệt, các đơn vị liên quan cần sớm làm rõ nguyên nhân khi có biến cố bất lợi nghiêm trọng, nhất là với những ca tử vong. Tình nguyện viên cần được tiêm sớm sau khi biết họ được tiêm vắc-xin hay giả dược.
Các thủ tục cấp kinh phí cho thử nghiệm lâm sàng vắc-xin Covid-19 nội sẽ được Vụ Kế hoạch – Tài chính làm đầu mối hướng dẫn.
Riêng với nghiên cứu thử nghiệm lâm sàng vắc-xin Nano Covax, Bộ đề nghị nhóm nghiên cứu và nhà sản xuất sớm cung cấp báo cáo dữ liệu về hiệu lực bảo vệ làm giảm trường hợp bệnh nặng và tử vong do Covid-19 và chịu trách nhiệm về số liệu, đảm bảo công khai, minh bạch, kịp thời bổ sung tiêm mũi tăng cường cho người tình nguyện.
Với nghiên cứu thử nghiệm lâm sàng vắc-xin ARCT-154, Thứ trưởng Bộ Y tế yêu cầu đơn vị liên quan báo cáo kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3.
Liên quan việc thử nghiệm lâm sàng vắc-xin S-268019, các tổ chức nhận thử phải đảm bảo tuân thủ đề cương nghiên cứu ở tất cả bước triển khai, tuyển chọn, quản lý, theo dõi, xử lý biến cố bất lợi, bảo đảm an toàn tuyệt đối cho người tham gia nghiên cứu.
Bộ Y tế cũng đồng ý mở rộng địa bàn triển khai, không hạn chế các địa phương tham gia, nhưng phải đảm bảo khoa học, chặt chẽ, hiệu quả.
Liên quan tới tiến độ của các loại vắc-xin nội, theo báo cáo của Bộ Y tế trình Thủ tướng đầu tháng 3, thời điểm đó Việt Nam đang có 3 ứng viên vắc-xin Covid-19 sản xuất trong nước và chuyển giao công nghệ đang triển khai thử nghiệm lâm sàng ở giai đoạn 2 và giai đoạn 3.
Vắc-xin Nanocovax của Công ty cổ phần công nghệ sinh học dược Nanogen đã nghiệm thu kết quả thử nghiệm lâm sàng giai đoạn 1 vào tháng 8/2021. Đã được Hội đồng đạo đức trong nghiên cứu y sinh học quốc gia đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3, với dữ liệu tính đến ngày 13/12/2021.
Hiện đang tiếp tục thu thập dữ liệu đánh giá tính an toàn, tính sinh miễn dịch và hiệu quả bảo vệ thử nghiệm lâm sàng giai đoạn 2 và giai đoạn 3 của vắc-xin theo đề cương nghiên cứu.
Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc và nguyên liệu làm thuốc đã họp thẩm định hồ sơ đăng ký lưu hành vắc-xin này và đề nghị công ty sản xuất, các đơn vị nghiên cứu khẳng định về tính chính xác của dữ liệu nghiên cứu.
Vắc-xin Covivac của Viện Vắc xin và sinh phẩm Nha Trang đã đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 1; đã hoàn thành tiêm 2 liều của thử nghiệm lâm sàng giai đoạn 2. Đã hoàn thành báo cáo giữa kỳ thử nghiệm lâm sàng giai đoạn 2, đang hoàn thiện đề cương thử nghiệm lâm sàng giai đoạn 3.
Vắc-xin Arct-154 là vắc xin mRNA của Công ty Acturus - Hoa Kỳ được chuyển giao công nghệ về Việt Nam, đã hoàn thành tiêm 2 mũi của thử nghiệm lâm sàng giai đoạn 2 và 3a, 3b, 3c.
Hiện doanh nghiệp đang thu thập, xử lý, phân tích dữ liệu nghiên cứu để đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 phục vụ xem xét cấp giấy đăng ký lưu hành trong trường hợp cấp bách.

-
Sốt xuất huyết tăng, TP.HCM và Hà Nội kích hoạt cao điểm chống dịch -
Tin mới y tế ngày 19/5: Mạng xã hội sẽ trở thành nguồn giám sát dịch bệnh truyền nhiễm -
Công nghệ lọc huyết tương kép hiện đại tiếp thêm hy vọng cho bệnh nhân mắc bệnh lý phức tạp -
Y tế số thay đổi cách người Việt chăm sóc sức khỏe mỗi ngày -
Thuốc đông y giả, quảng cáo sai sự thật nở rộ trên mạng xã hội -
Nhà thuốc Đông y Đức nguyên Đường thực hiện lời dạy “Lương y như từ mẫu” của Bác Hồ -
Bộ Y tế thúc đẩy thực thi nghiêm Luật Phòng, chống tác hại thuốc lá
-
 Greenfeed mở rộng hệ sinh thái nông nghiệp với nhà máy 12.000 m2 tại TP. Đồng Nai
Greenfeed mở rộng hệ sinh thái nông nghiệp với nhà máy 12.000 m2 tại TP. Đồng Nai -
 Searefico: Lợi nhuận phục hồi mạnh, backlog kỷ lục - Sẵn sàng cho chu kỳ tăng trưởng mới
Searefico: Lợi nhuận phục hồi mạnh, backlog kỷ lục - Sẵn sàng cho chu kỳ tăng trưởng mới -
 Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành du lịch
Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành du lịch -
 Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành Tài chính - Chứng khoán
Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành Tài chính - Chứng khoán -
 Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành nông nghiệp công nghệ cao
Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành nông nghiệp công nghệ cao -
 Kredivo Group mua lại Timo – nền tảng ngân hàng số tiên phong tại Việt Nam
Kredivo Group mua lại Timo – nền tảng ngân hàng số tiên phong tại Việt Nam














