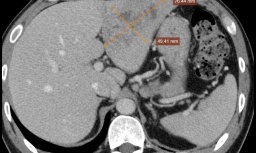
 Bác sỹ cảnh báo nguy cơ áp xe gan từ thói quen ăn rau sống
Bác sỹ cảnh báo nguy cơ áp xe gan từ thói quen ăn rau sống -
 Bác sỹ cảnh báo nguy cơ áp xe gan từ thói quen ăn rau sống
Bác sỹ cảnh báo nguy cơ áp xe gan từ thói quen ăn rau sống -
 Tăng cường năng lực y tế dự phòng cho vùng biển đảo
Tăng cường năng lực y tế dự phòng cho vùng biển đảo -
 Tin mới y tế ngày 17/5: WHO cảnh báo gánh nặng tăng huyết áp toàn cầu ngày càng nghiêm trọng
Tin mới y tế ngày 17/5: WHO cảnh báo gánh nặng tăng huyết áp toàn cầu ngày càng nghiêm trọng -
 Y tế số và cuộc cách mạng dữ liệu đang thay đổi ngành y Việt Nam
Y tế số và cuộc cách mạng dữ liệu đang thay đổi ngành y Việt Nam -
Người Việt tiêu thụ muối gần gấp đôi mức khuyến cáo của Tổ chức Y tế thế giới -
Tin mới y tế ngày 16/5: Xây dựng “bộ khung chuẩn” cho bác sỹ y học cổ truyền
Trong số gần 800 loại được gia hạn lần này có 730 thuốc được gia hạn theo quy định của Luật Dược năm 2016 và 35 thuốc có chứng minh tương đương sinh học được công bố.
.jpeg) |
| Ảnh minh họa |
Đối với 730 thuốc được gia hạn đợt này có 453 thuốc được gia hạn trong 5 năm; 219 thuốc gia hạn trong 3 năm và 58 thuốc gia hạn đến ngày 31/12/2025.
Được biết, các sản phẩm thuốc được gia hạn giấy đăng ký lưu hành lần này đều là thuốc sản xuất trong nước, khá đa dạng về nhóm tác dụng dược lý gồm thuốc điều trị tim mạch, tăng huyết áp, đái tháo đường, điều trị ung thư, thuốc kháng virus, thuốc điều trị bệnh lý đường hô hấp, thuốc kháng sinh, hạ sốt, giảm đau, kháng viêm thông thường khác....
Được biết, trong tháng 8/2024, Cục Quản lý Dược đã liên tục có các đợt gia hạn, cấp mới giấy đăng ký lưu thành thuốc, vắc-xin và sinh phẩm y tế theo Luật Dược.
Trong đó, đợt mới đây nhất, khoảng 10 ngày trước đã có gần 900 sản phẩm thuốc, bao gồm cả biệt dược gốc, vắc-xin, sinh phẩm y tế, trong đó danh mục thuốc biệt dược gốc gồm 30 loại, danh mục thuốc sản xuất trong nước gồm gần 400 loại, số còn lại là danh mục thuốc nước ngoài.
Trong số này có cả biệt dược, vắc-xin và sinh phẩm y tế được cấp mới, gia hạn trong thời gian 5 năm; 3 năm và đến hết ngày 31/12/2025.
Ngoài ra Cục Quản lý Dược cũng tiến hành gia hạn giấy đăng ký lưu hành thuốc theo Nghị quyết 80 của Quốc hội.
Tình trạng thiếu thuốc chữa bệnh thời gian qua liên quan khá lớn đến việc cấp phép mới, gia hạn đăng ký lưu hành thuốc, nguyên liệu làm thuốc.
Vì vậy theo đại diện Bộ Y tết, dự thảo Luật Dược sửa đổi đã đơn giản hóa hồ sơ gia hạn, thay đổi, bổ sung giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc. Tinh giản thủ tục hành chính, giảm thời gian gia hạn, cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc.
Về hồ sơ, trình tự, thủ tục gia hạn hiệu lực giấy đăng ký lưu hành đối với thuốc, nguyên liệu làm thuốc: Khoản 1 Điều 56 Luật Dược 2016 quy định tất cả các thuốc sau khi hết hạn hiệu lực Giấy đăng ký lưu hành, đều phải nộp lại hồ sơ gia hạn và các hồ sơ này đều phải trải qua quá trình thẩm định, xét duyệt của Hội đồng tư vấn cấp Giấy đăng ký lưu hành. Quy định này của Luật Dược đã góp phần giúp cho việc quản lý thuốc có chất lượng, an toàn và hiệu quả.
Tuy nhiên, quy định chỉ phù hợp với các thuốc trong quá trình lưu hành có vấn đề về chất lượng hoặc an toàn cần phải đánh giá lại trước khi gia hạn hiệu lực giấy đăng ký lưu hành.
Bên cạnh đó, tại dự thảo Luật Dược sửa đổi, ban soạn thảo đã đề xuất quy định các trường hợp gia hạn, thay đổi, bổ sung Giấy đăng ký lưu hành không phải thông qua Hội đồng tư vấn cấp Giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc hoặc không phải phê duyệt.
Giảm thời gian giải quyết hồ sơ từ 3 tháng xuống còn 15 ngày làm việc đối với hồ sơ thay đổi, bổ sung chỉ cần công bố.
Bổ sung quy định cho phép cơ sở được tiếp tục sử dụng giấy đăng ký lưu hành sau khi hết hiệu lực và đã nộp hồ sơ gia hạn theo quy định đến khi được gia hạn hoặc có văn bản của Bộ Y tế.
Bổ sung quy định cho phép thay thế CPP (Giấy chứng nhận sản phẩm dược) bằng giấy tờ pháp lý chứng minh thuốc được cấp phép trong trường hợp đáp ứng nhu cầu phòng, chống dịch bệnh…

-
Y tế số và cuộc cách mạng dữ liệu đang thay đổi ngành y Việt Nam -
Người Việt tiêu thụ muối gần gấp đôi mức khuyến cáo của Tổ chức Y tế thế giới -
Tin mới y tế ngày 16/5: Xây dựng “bộ khung chuẩn” cho bác sỹ y học cổ truyền -
TP.HCM hỗ trợ toàn diện Bệnh viện Bà Rịa, hướng tới bệnh viện cửa ngõ phía Đông Nam -
Tuần Lễ Vàng 2026 - Tiếp thêm hy vọng cho các gia đình hiếm muộn -
Dịch sốt xuất huyết tăng cao, chuyên gia cảnh báo biến chứng nặng của bệnh -
Tin mới y tế ngày 15/5: Giảm nguy cơ lây bệnh lao trong cộng đồng
-
 Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành công nghệ - viễn thông - chuyển đổi số
Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành công nghệ - viễn thông - chuyển đổi số -
 Công bố Top 10 Doanh nghiệp Bán lẻ Đổi mới sáng tạo và Kinh doanh hiệu quả năm 2026
Công bố Top 10 Doanh nghiệp Bán lẻ Đổi mới sáng tạo và Kinh doanh hiệu quả năm 2026 -
 Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành Thực phẩm - Đồ uống
Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành Thực phẩm - Đồ uống -
 Thấp tầng khan hiếm phía Tây Hà Nội: An khánh Ecomony và dư địa tăng giá tại Bắc An Khánh
Thấp tầng khan hiếm phía Tây Hà Nội: An khánh Ecomony và dư địa tăng giá tại Bắc An Khánh -
 EVF công bố bổ nhiệm nhân sự cấp cao
EVF công bố bổ nhiệm nhân sự cấp cao -
 Hoàng Thu Hiền: Kinh doanh món ăn gia đình bằng sự tử tế và cái tâm của người làm mẹ
Hoàng Thu Hiền: Kinh doanh món ăn gia đình bằng sự tử tế và cái tâm của người làm mẹ