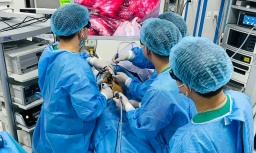
 Tin mới y tế ngày 6/5: Phẫu thuật nội soi 3D cứu hai ca ung thư thực quản phức tạp
Tin mới y tế ngày 6/5: Phẫu thuật nội soi 3D cứu hai ca ung thư thực quản phức tạp -
 Tin mới y tế ngày 6/5: Phẫu thuật nội soi 3D cứu hai ca ung thư thực quản phức tạp
Tin mới y tế ngày 6/5: Phẫu thuật nội soi 3D cứu hai ca ung thư thực quản phức tạp -
 MEDLATEC miễn phí bộ 3 xét nghiệm đánh giá mức độ hủy hoại tế bào gan, giảm 50% siêu âm đàn hồi mô gan
MEDLATEC miễn phí bộ 3 xét nghiệm đánh giá mức độ hủy hoại tế bào gan, giảm 50% siêu âm đàn hồi mô gan -
 Bộ Y tế cảnh báo khẩn vi rút Hanta lây truyền từ chuột
Bộ Y tế cảnh báo khẩn vi rút Hanta lây truyền từ chuột -
 Góc hàm sưng to phát hiện u tuyến nước bọt hiếm gặp
Góc hàm sưng to phát hiện u tuyến nước bọt hiếm gặp -
Cắt giảm hàng trăm điều kiện kinh doanh trong lĩnh vực y tế -
Tin mới y tế ngày 5/5: Thu hồi 3 lô sữa a2 Platinum Premium dành cho trẻ sơ sinh, cảnh báo nguy cơ độc tố
Vắc-xin Moderna do Công ty Rovi Pharma Industrial Services, S.A, Tây Ban Nha và Recipharm Monts, Pháp sản xuất và được chi nhánh Công ty TNHH Zuellig Pharma Việt Nam đề xuất phê duyệt gửi Bộ Y tế Việt Nam.
 |
| Bộ Y tế phê duyệt có điều kiện vắc-xin cho nhu cầu cấp bách trong phòng, chống dịch bệnh Covid-19 đối với vắc-xin Spikevax - tên khác là vắc-xin Moderna. |
Vắc-xin Moderna được phê duyệt dựa trên dữ liệu an toàn, chất lượng và hiệu quả do Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam cung cấp cho Bộ Y tế Việt Nam tính đến ngày 23/6/2021 và cam kết của Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam về tính chính xác của các tài liệu đã cung cấp cho Bộ Y tế Việt Nam.T
Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam có trách nhiệm phối hợp với cơ sở sản xuất vắc-xin phản hồi kịp thời các yêu cầu từ Bộ Y tế Việt Nam để bổ sung thêm dữ liệu hoặc các yêu cầu khác có liên quan đến vắc-xin Moderna và chủ động cung cấp, cập nhật các thông tin mới có liên quan đến vắc-xin Moderna cho Bộ Y tế Việt Nam trong suốt quá trình phát triển sản phẩm;
Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam chịu trách nhiệm phối hợp với cơ sở sản xuất vắc-xin đảm bảo các điều kiện sản xuất tại cơ sở sản xuất vắc-xin Moderna nhập khẩu vào Việt Nam và đảm bảo an toàn, hiệu quả và chất lượng của lô vắc-xin Moderna nhập khẩu vào Việt Nam; Phối hợp với đơn vị phân phối, sử dụng vắc-xin Moderna triển khai hệ thống cảnh giác dược toàn diện đối với vắc-xin này tại Việt Nam theo quy định của pháp luật;
Bộ Y tế yêu cầu Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam phối hợp với Cục Khoa học công nghệ và Đào tạo và đơn vị có đủ điều kiện tổ chức thực hiện việc đánh giá tính an toàn, hiệu quả của vắc-xin Moderna trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vắc-xin, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng;
Phối hợp với Viện Kiểm định Quốc gia vắc-xin và sinh phẩm y tế trong việc kiểm định các lô vắc-xin Moderna trước khi đưa ra sử dụng; phối hợp với Cục Y tế dự phòng hướng dẫn việc bảo quản, phân phối và sử dụng vắc-xin Moderna cho các cơ sơ tiêm chủng.
Ngoài ra, Bộ Y tế cũng yêu cầu Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam phải phối hợp với Bộ Y tế Việt Nam để triển khai quản trị rủi ro đối với vắc-xin Moderna trong suốt quá trình lưu hành tại Việt Nam. Đồng thời, việc sử dụng vắc-xin Moderna phải theo hướng dẫn của Bộ Y tế Việt Nam.
Về phía cơ quan quản lý nhà nước, Bộ Y tế yêu cầu Cục Quản lý Dược có trách nhiệm cấp phép nhập khẩu vắc-xin Moderna theo quy định tại Điều 67 Nghị định 54/2017/NĐ-CP.
Cục Khoa học công nghệ và Đào tạo có trách nhiệm lựa chọn đơn vị có đủ điều kiện đánh giá tính an toàn, hiệu quả của vắc-xin trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vắc-xin, sinh phẩm y tế của Bộ Y tế.
Cục Y tế Dự phòng thực hiện các trách nhiệm liên quan đến tiêm chủng vắc-xin Moderna theo quy định. Viện Kiểm định Quốc gia vắc-xin và sinh phẩm y tế có trách nhiệm tiến hành kiểm định và cấp Giấy chứng nhận xuất xưởng lô vắc-xin Moderna trước khi đưa ra sử dụng.
Theo các chuyên gia, hiệu quả của vắc-xin Moderna trong nghiên cứu được đánh giá bằng tiêu chí giảm tỷ lệ bệnh nhân mắc Covid-19 có triệu chứng (tính từ thời điểm 14 ngày sau khi hoàn thành liều tiêm thứ 2).
Nghiên cứu trên 28.207 bệnh nhân (độ tuổi từ 18 đến 94) cho thấy vắc-xin Moderna có hiệu quả giảm 94.1% nguy cơ mắc Covid-19 có triệu chứng.
Các tác dụng không mong muốn thường hay xuất hiện hơn sau liều tiêm thứ 2. Theo đó, các phản ứng phụ này thường có mức độ từ nhẹ đến trung bình và các triệu chứng thường cải thiện sau khoảng 2 - 3 ngày sau tiêm vắc-xin. Các tác dụng không mong muốn thường gặp nhất bao gồm: Đau vị trí tiêm (92.0%); Mệt mỏi (70.0%); Đau đầu (64.7%); Đau cơ, khớp (~ 50%); Nôn, buồn nôn (23.0%); Sốt (15.5%)
Tỷ lệ xảy ra phản ứng sốc phản vệ (nguy cơ đe dọa tính mạng) sau tiêm vắc-xin được ghi nhận là 2.8 ca/1 triệu liều.
Đối tượng cần cẩn trọng khi tiêm vắc-xin Moderna là người có tiền sử phản ứng dị ứng nghiêm trọng (như phản vệ) với liều vaccin mRNA Covid-19 trước đó.
Có tiền sử phản ứng quá mẫn (bao gồm các triệu chứng mày đay cấp tính, phù mạch, suy hô hấp, phản vệ trong vòng 4 giờ sau tiêm với polyethylene glycol (PEG) hoặc polysorbate
Ngoài ra, cần chú ý thận trọng khi tiêm vắc-xin Moderna nếu bệnh nhân đang có các bệnh lý cấp tính mức độ trung bình đến nặng hoặc có tiền sử quá mẫn với các vắc-xin khác hoặc các thuốc khác. Các trường hợp này nếu cần tiêm vắc-xin cần xin ý kiến của chuyên gia miễn dịch-dị ứng.
Vắc-xin Moderna được chỉ định tiêm bắp liều 0.5 ml (chứa 100 μg of mRNA-1273). Tiêm tổng cộng 2 liều, mỗi liều tiêm cách nhau tối thiểu 28 ngày.
Về quá trình nghiên cứu, sản xuất vắc-xin Moderna
Tháng 1/2020, Moderna bắt đầu nghiên cứu vắc-xin coronavirus.
Ngày 16/3, các nhà khoa học Moderna lần đầu tiên thử nghiệm vắc-xin Covid-19 trên người.
Ngày16/4, Moderna thông báo rằng chính phủ Hoa Kỳ sẽ cung cấp 483 triệu đô la hỗ trợ cho việc phát triển và thử nghiệm vắc xin của Moderna. Các nhà nghiên cứu của Viện Y tế Quốc gia sẽ giám sát phần lớn nghiên cứu, bao gồm việc thử nghiệm lâm sàng.
Ngày 27/7, Sau khi các nghiên cứu ban đầu mang lại kết quả đầy hứa hẹn, Moderna và N.I.H. bắt đầu thử nghiệm Giai đoạn 3 trên 30.000 tình nguyện viên ở khắp Hoa Kỳ. Trong đó 1/4 số người tham gia là từ 65 tuổi trở lên.
Ngày 28/7, Moderna phát hiện rằng vắc-xin có thể chống coronavirus ở khỉ.
Ngày 11/8, Chính phủ Hoa Kỳ thưởng cho công ty thêm 1,5 tỷ đô la để đổi lấy 100 triệu liều, nếu vắc xin được Cục Quản lý Thực phẩm và Dược phẩm cấp phép.
Ngày 16/11, Moderna công bố dữ liệu sơ bộ về kết quả thử nghiệm giai đoạn 3. Các nhà nghiên cứu ước tính rằng vắc-xin có thể đạt hiệu quả đến 94,1%, cao hơn nhiều so với dự kiến của các chuyên gia khi bắt đầu thử nghiệm vắc-xin.
Ngày 30/11, Moderna xin cấp phép sử dụng khẩn cấp từ F.D.A.
Ngày 2/12, Moderna đăng ký thử nghiệm vắc-xin trên trẻ em từ 12 đến 18 tuổi.
Ngày 18/12, F.D.A. cấp phép sử dụng vắc xin Moderna trong trường hợp khẩn cấp. Những mũi tiêm vắc xin đầu tiên bắt đầu vào ngày 21 tháng 12.
Ngày 23/12, Canada cấp phép sử dụng vắc xin.
Ngày 31/12, Công ty dự kiến sản xuất 20 triệu liều vào cuối năm nay và lên đến một tỷ liều vào năm 2021. Mỗi người tiêm chủng sẽ cần hai liều.
Ngày 4/1, Israel cấp phép sử dụng vắc xin trong trường hợp khẩn cấp.
-
Cắt giảm hàng trăm điều kiện kinh doanh trong lĩnh vực y tế -
Tin mới y tế ngày 5/5: Thu hồi 3 lô sữa a2 Platinum Premium dành cho trẻ sơ sinh, cảnh báo nguy cơ độc tố -
Trẻ nguy kịch vì sơ cứu đuối nước sai cách -
Tin mới y tế ngày 4/5: Từ 15/5, chậm đóng, trốn đóng bảo hiểm y tế có thể bị phạt tới 70 triệu đồng -
Bịt lỗ hổng chuỗi thực phẩm để ngăn ngừa ngộ độc -
Bệnh não mô cầu: Tỷ lệ tử vong cao, biến chứng ở mức nguy hiểm -
Tin mới y tế ngày 3/5: Cảnh báo thuốc đông y gia truyền giả, nhiều người “tiền mất, tật mang”
-
 Nutifood tài trợ 9,3 tỷ đồng cho đội Bóng chuyền nữ TP.HCM, tiếp sức trở lại đỉnh cao
Nutifood tài trợ 9,3 tỷ đồng cho đội Bóng chuyền nữ TP.HCM, tiếp sức trở lại đỉnh cao -
 Cập nhật giá đơn vị Quỹ liên kết đơn vị của AIA Việt Nam ngày 6/5/2026
Cập nhật giá đơn vị Quỹ liên kết đơn vị của AIA Việt Nam ngày 6/5/2026 -
 Xe máy điện Việt Nam: Ai hiểu người dùng sẽ thắng
Xe máy điện Việt Nam: Ai hiểu người dùng sẽ thắng -
 Ambience: Từ chỗ ở đến không gian sống đa trải nghiệm
Ambience: Từ chỗ ở đến không gian sống đa trải nghiệm -
 Agribank tiếp lực doanh nghiệp bứt phá tăng trưởng năm 2026
Agribank tiếp lực doanh nghiệp bứt phá tăng trưởng năm 2026 -
 FE CREDIT: Khi mảnh ghép chiến lược kích hoạt cộng hưởng hệ sinh thái VPBank
FE CREDIT: Khi mảnh ghép chiến lược kích hoạt cộng hưởng hệ sinh thái VPBank