Virus Hanta và cảnh báo phòng dịch từ sớm tại Việt Nam
Virus Hanta và cảnh báo phòng dịch từ sớm tại Việt Nam -
 Virus Hanta và cảnh báo phòng dịch từ sớm tại Việt Nam
Virus Hanta và cảnh báo phòng dịch từ sớm tại Việt Nam -
 Liên tiếp trẻ bị chó cắn phải nhập viện, cảnh báo nguy cơ bệnh dại bùng phát
Liên tiếp trẻ bị chó cắn phải nhập viện, cảnh báo nguy cơ bệnh dại bùng phát -
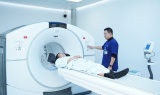 Tin mới y tế ngày 10/5: Cập nhật xu hướng điều trị ung thư hiện đại
Tin mới y tế ngày 10/5: Cập nhật xu hướng điều trị ung thư hiện đại -
 Bộ Y tế khuyến cáo phòng bệnh do virus Hanta
Bộ Y tế khuyến cáo phòng bệnh do virus Hanta -
Khoảng 5-25% người khỏe mạnh có thể mang não mô cầu mà không biết -
Tin mới y tế ngày 9/5: Trẻ dưới 6 tuổi sẽ được khám định kỳ hằng năm, có tầm soát nguy cơ tự kỷ
Theo Bộ Y tế, thời gian qua, công tác kiểm tra, giám sát chất lượng thuốc đã phát hiện một số hành vi vi phạm liên quan đến hồ sơ đăng ký thuốc và quy định pháp lý trong sản xuất, kinh doanh dược phẩm.
 |
| Ảnh minh họa. |
Để khắc phục tình trạng này, Cục Quản lý Dược đã ban hành văn bản yêu cầu các Sở Y tế và các cơ sở sản xuất thuốc trên cả nước thực hiện nghiêm nhiều nội dung quan trọng.
Đối với các cơ sở sản xuất, Bộ Y tế yêu cầu phải duy trì và tuân thủ nghiêm ngặt các nguyên tắc, tiêu chuẩn "Thực hành tốt sản xuất thuốc" (GMP) trong toàn bộ quá trình sản xuất, bao gồm cả trường hợp sản xuất thực phẩm bảo vệ sức khỏe trên cùng dây chuyền.
Đặc biệt, việc kiểm soát chặt chẽ nguồn gốc và chất lượng nguyên liệu làm thuốc được đặt lên hàng đầu. Nguyên liệu đầu vào phải có nguồn gốc rõ ràng, đúng với thông tin đã đăng ký trong hồ sơ lưu hành, được cung cấp từ các đơn vị đã qua thẩm định, và đạt tiêu chuẩn chất lượng theo phê duyệt của Bộ Y tế trước khi đưa vào sản xuất.
Các cơ sở sản xuất cũng phải rà soát toàn bộ quy trình sản xuất, hồ sơ kiểm nghiệm và hồ sơ lưu hành, đảm bảo mọi khâu tuân thủ đúng quy định đã được cấp phép.
Trường hợp cần thay đổi quy trình sản xuất, tiêu chuẩn chất lượng hay phương pháp phân tích, doanh nghiệp phải thực hiện đầy đủ thủ tục đăng ký thay đổi và chỉ được triển khai sau khi được Bộ Y tế phê duyệt.
Bộ Y tế khuyến khích các cơ sở xây dựng hệ thống quản lý chất lượng toàn diện, kiểm soát mọi hoạt động sản xuất theo các tiêu chuẩn GMP, GLP, GSP.
Đồng thời, các doanh nghiệp phải thực hiện công tác tự kiểm tra, rà soát định kỳ để kịp thời phát hiện và khắc phục sai sót. Trách nhiệm về chất lượng và độ an toàn của sản phẩm, bao gồm cả thuốc và thực phẩm bảo vệ sức khỏe, hoàn toàn thuộc về cơ sở sản xuất.
Ngoài ra, khi phát hiện bất kỳ vấn đề nào liên quan đến chất lượng, an toàn sản phẩm, các đơn vị phải báo cáo kịp thời với Bộ Y tế và Sở Y tế địa phương để có biện pháp xử lý phù hợp.
Cục Quản lý Dược cũng yêu cầu Sở Y tế các tỉnh, thành phố tăng cường thanh tra, giám sát cơ sở sản xuất thuốc, đặc biệt là các đơn vị, đồng thời sản xuất thực phẩm bảo vệ sức khỏe và mỹ phẩm.
Việc giám sát cần bao gồm kiểm tra tuân thủ quy định về sử dụng nguyên liệu, ghi nhãn, quảng cáo sản phẩm, và thực hiện đúng các nguyên tắc GMP, GSP trong bảo quản, sản xuất.
Các trường hợp vi phạm phải bị xử lý nghiêm theo quy định của pháp luật, đồng thời báo cáo lên Bộ Y tế để có biện pháp can thiệp kịp thời và đồng bộ.
-
Khoảng 5-25% người khỏe mạnh có thể mang não mô cầu mà không biết -
Tin mới y tế ngày 9/5: Trẻ dưới 6 tuổi sẽ được khám định kỳ hằng năm, có tầm soát nguy cơ tự kỷ -
Người đàn ông phát hiện mắc viêm gan B mạn tính và xơ hóa gan khi kiểm tra sức khỏe định kỳ tại MEDLATEC -
Ðại diện Việt Nam 2 năm liên tiếp thắng lớn tại Healthcare Asia Pharma Awards -
Hoại tử, áp xe môi sau tiêm tan filler tại cơ sở làm đẹp không phép -
Chấm dứt cơn đau vai suốt 10 năm nhờ liệu pháp sinh học hiện đại -
Đề xuất thống nhất một đầu mối quản lý an toàn thực phẩm toàn quốc
-
 Diamond Hill Thái Nguyên khai trương tầng thực tế, hiện thực hóa chuẩn sống cao cấp giữa trung tâm thành phố
Diamond Hill Thái Nguyên khai trương tầng thực tế, hiện thực hóa chuẩn sống cao cấp giữa trung tâm thành phố -
 Đầu tư phòng thí nghiệm dược: Khi thiết bị chưa đủ để tạo hiệu quả
Đầu tư phòng thí nghiệm dược: Khi thiết bị chưa đủ để tạo hiệu quả -
 CARA Lighting phát triển giải pháp chiếu sáng gắn với sức khỏe và trải nghiệm
CARA Lighting phát triển giải pháp chiếu sáng gắn với sức khỏe và trải nghiệm -
 VSIP ký kết hợp tác phân phối dự án Sun Casa Square và triển khai chuỗi tiện ích
VSIP ký kết hợp tác phân phối dự án Sun Casa Square và triển khai chuỗi tiện ích -
 Acecook Việt Nam khởi động dự án trồng 10.500 cây xanh tại tỉnh Quảng Trị - “Gieo mầm hạnh phúc - phủ xanh tương lai”
Acecook Việt Nam khởi động dự án trồng 10.500 cây xanh tại tỉnh Quảng Trị - “Gieo mầm hạnh phúc - phủ xanh tương lai” -
 Giao lưu nhân dân tại Đồng Nai chào mừng 50 năm quan hệ Việt Nam - Thái Lan
Giao lưu nhân dân tại Đồng Nai chào mừng 50 năm quan hệ Việt Nam - Thái Lan