Trục lợi quỹ bảo hiểm y tế sẽ bị xử lý nghiêm theo quy định mới
Trục lợi quỹ bảo hiểm y tế sẽ bị xử lý nghiêm theo quy định mới -
 Trục lợi quỹ bảo hiểm y tế sẽ bị xử lý nghiêm theo quy định mới
Trục lợi quỹ bảo hiểm y tế sẽ bị xử lý nghiêm theo quy định mới -
 Tin mới y tế ngày 24/5: Suy tim vì lạm dụng thuốc giảm đau
Tin mới y tế ngày 24/5: Suy tim vì lạm dụng thuốc giảm đau -
 WHO đánh giá nguy cơ Ebola xâm nhập Việt Nam
WHO đánh giá nguy cơ Ebola xâm nhập Việt Nam -
 MEDLATEC chẩn đoán sớm, điều trị thành công bệnh nhân nhiễm khuẩn huyết nặng trên nền đái tháo đường type 2
MEDLATEC chẩn đoán sớm, điều trị thành công bệnh nhân nhiễm khuẩn huyết nặng trên nền đái tháo đường type 2 -
Hiểu đúng về vắc-xin HPV để bảo vệ trước nguy cơ ung thư -
Mở “luồng xanh” phát triển doanh nghiệp y tế công nghệ cao
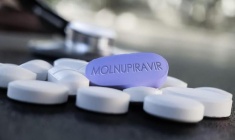
Cục Quản lý Dược, Bộ Y tế ban hành Quyết định số 69/QĐ-QLD về việc cấp phép cho 3 loại thuốc chứa Molnupiravir được sản xuất trong nước, phục vụ công tác phòng, chống dịch Covid-19. Việc cấp phép cho các loại thuốc này có hiệu lực 3 năm từ ngày ký ban hành quyết định.
| Cục Quản lý Dược, Bộ Y tế đã cấp phép cho 3 loại thuốc chứa Molnupiravir được sản xuất trong nước, phục vụ công tác phòng, chống dịch Covid-19. |
Theo đó, 3 loại thuốc được Cục Quản lý Dược cấp phép, bao gồm: Molravir 400: Hàm lượng Molnupiravir 400mg, dạng viên nang cứng, tuổi thọ 6 tháng, do Công ty cổ phần Dược phẩm Boston Việt Nam sản xuất;
Movinavir: Hàm lượng 200mg Molnupiravir, dạng viên nang cứng, tuổi thọ 6 tháng, do Công ty Cổ phần Hóa dược phẩm Mekophar sản xuất;
Molnuporavir Stella 400: Hàm lượng 400mg Molnupiravir, dạng viên nang cứng, tuổi thọ 8 tháng, do Công ty TNHH Liên doanh Stellapharm - chi nhánh 1 sản xuất.
Cục Quản lý Dược yêu cầu các cơ sở sản xuất và cơ sở đăng ký thuốc sản xuất phối hợp với các cơ sở điều trị thực hiện đúng các quy định hiện hành về thuốc kê đơn, theo dõi an toàn, hiệu quả, tác dụng không mong muốn của thuốc trên người Việt Nam và tổng hợp, báo cáo theo quy định.
Ngoài ra, Cục Quản lý Dược cũng đề nghị, Sở Y tế các tỉnh, thành phố trực thuộc Trung ương thông báo cho cơ sở khám, chữa bệnh, các cán bộ y tế, cơ sở cung ứng thuốc trên địa bàn thông báo cho bệnh nhân về các lợi ích, rủi ro khi sử dụng thuốc, các phương pháp điều trị, các thuốc khác có thể thay thế Molnupiravir trong điều trị Covid-19.
Cùng với đó, tăng cường theo dõi, giám sát, phát hiện các trường hợp xảy ra phản ứng có hại của thuốc (nếu có), gửi báo cáo về Trung tâm quốc gia về thông tin thuốc và theo dõi phản ứng có hại của thuốc (Hà Nội) hoặc Trung tâm khu vực về thông tin thuốc và theo dõi phản ứng có hại của thuốc TP.HCM) theo quy định.
Theo Cục Quản lý Dược, trách nhiệm của cơ sở sản xuất và cơ sở đăng ký phải thực hiện kiểm tra chất lượng nguyên liệu theo tiêu chuẩn nhà sản xuất và phải đạt yêu cầu mới được đưa vào sản xuất, đồng thời thực hiện việc lấy mẫu kiểm tra chất lượng theo tiêu chuẩn; thực hiện theo dõi về chất lượng, an toàn, hiệu quả của thuốc khi đưa ra lưu hành trên thị trường.
Trong quá trình lưu hành thuốc, căn cứ vào việc theo dõi, cập nhật thông tin về độ an toàn, hiệu quả của 3 loại thuốc trên, Cục Quản lý dược có thể quyết định thu hồi giấy đăng ký lưu hành đã cấp này theo quy định của Luật Dược.
Vừa qua, Molnupiravir được thử nghiệm lâm sàng cho khoảng 80.000 bệnh nhân tại 51 tỉnh, thành phố trên cả nước.
Kết quả được Bộ Y tế công bố khi điều trị F0 trong cộng đồng, cho thấy Molnupiravir có tính an toàn cao, dung nạp tốt, hiệu quả rõ rệt về giảm tải lượng virus, giảm lây lan, giảm chuyển nặng, rút ngắn thời gian điều trị với tỷ lệ bệnh nhân có kết quả xét nghiệm RT-PCR sau 5 ngày âm tính; tỷ lệ chuyển nặng rất thấp từ 0,02%-0,06% và không có ca nào dẫn đến tử vong.
Bộ Y tế cũng cho biết thuốc kháng virus Molnupiravir được sử dụng để điều trị Covid-19 mức độ nhẹ đến trung bình ở người trưởng thành dương tính với xét nghiệm chẩn đoán SARS-CoV-2 và có ít nhất 1 yếu tố nguy cơ làm bệnh tiến triển nặng.
Molnupiravir dùng trên bệnh nhân có thời gian khởi phát triệu chứng dưới 5 ngày, không được sử dụng quá 5 ngày liên tiếp; không được sử dụng để dự phòng sau hay trước phơi nhiễm để phòng Covid-19.
Đối với phụ nữ có thai và cho con bú, Molnupiravir không được khuyến cáo sử dụng trong thời kỳ mang thai. Phụ nữ có khả năng mang thai nên sử dụng biện pháp tránh thai hiệu quả trong thời gian điều trị và trong 4 ngày sau liều Molnupiravir cuối cùng.
Dựa trên khả năng xảy ra các phản ứng có hại cho trẻ sơ sinh từ Molnupiravir, không khuyến cáo cho con bú trong thời gian điều trị và trong 4 ngày sau liều Molnupiravir cuối cùng.
Đối với trẻ em và thanh thiếu niên, Molnupiravir không được phép sử dụng cho bệnh nhân dưới 18 tuổi vì có thể ảnh hưởng đến sự phát triển của xương và sụn.
-
Hiểu đúng về vắc-xin HPV để bảo vệ trước nguy cơ ung thư -
Mở “luồng xanh” phát triển doanh nghiệp y tế công nghệ cao -
Tin mới y tế ngày 23/5: Nhiều bệnh lý của mắt nguy hiểm bị phát hiện muộn, nguy cơ mù lòa gia tăng -
Y học tái tạo bước vào giai đoạn bùng nổ, bệnh viện Việt Nam tăng tốc hội nhập quốc tế -
Bộ Y tế đề xuất nhiều chính sách mới để kiểm soát thuốc lá -
Bộ Y tế yêu cầu sẵn sàng mọi kịch bản trước nguy cơ Ebola xâm nhập -
WHO vinh danh Việt Nam vì thành tựu phòng, chống tác hại thuốc lá
-
Hệ thống Trường quốc tế Hoa Kỳ APU ghi dấu ấn với 30 triệu USD học bổng cho học sinh tốt nghiệp năm 2026
-
 Vinacomin và Tập đoàn Marubeni (Nhật Bản): Thúc đẩy hợp tác toàn diện và bền vững
Vinacomin và Tập đoàn Marubeni (Nhật Bản): Thúc đẩy hợp tác toàn diện và bền vững -
 Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành Vật liệu xây dựng
Công bố Top 10 Doanh nghiệp Đổi mới sáng tạo và Kinh doanh hiệu quả 2026 ngành Vật liệu xây dựng -
 Nhơn Trạch 3 và Nhơn Trạch 4: Dấu ấn nổi bật của PV Power năm 2025
Nhơn Trạch 3 và Nhơn Trạch 4: Dấu ấn nổi bật của PV Power năm 2025 -
 Cơ hội trúng 500 triệu đồng khi gửi tiền dự thưởng trên Agribank Plus
Cơ hội trúng 500 triệu đồng khi gửi tiền dự thưởng trên Agribank Plus -
 SeABank thông báo mời thầu
SeABank thông báo mời thầu