Tin mới y tế ngày 9/5: Trẻ dưới 6 tuổi sẽ được khám định kỳ hằng năm, có tầm soát nguy cơ tự kỷ
Tin mới y tế ngày 9/5: Trẻ dưới 6 tuổi sẽ được khám định kỳ hằng năm, có tầm soát nguy cơ tự kỷ -
 Tin mới y tế ngày 9/5: Trẻ dưới 6 tuổi sẽ được khám định kỳ hằng năm, có tầm soát nguy cơ tự kỷ
Tin mới y tế ngày 9/5: Trẻ dưới 6 tuổi sẽ được khám định kỳ hằng năm, có tầm soát nguy cơ tự kỷ -
 Người đàn ông phát hiện mắc viêm gan B mạn tính và xơ hóa gan khi kiểm tra sức khỏe định kỳ tại MEDLATEC
Người đàn ông phát hiện mắc viêm gan B mạn tính và xơ hóa gan khi kiểm tra sức khỏe định kỳ tại MEDLATEC -
 Ðại diện Việt Nam 2 năm liên tiếp thắng lớn tại Healthcare Asia Pharma Awards
Ðại diện Việt Nam 2 năm liên tiếp thắng lớn tại Healthcare Asia Pharma Awards -
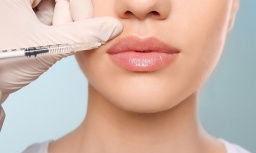
 Hoại tử, áp xe môi sau tiêm tan filler tại cơ sở làm đẹp không phép
Hoại tử, áp xe môi sau tiêm tan filler tại cơ sở làm đẹp không phép -
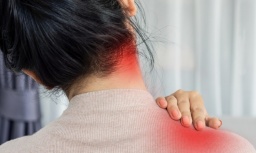
Chấm dứt cơn đau vai suốt 10 năm nhờ liệu pháp sinh học hiện đại -
Đề xuất thống nhất một đầu mối quản lý an toàn thực phẩm toàn quốc
Xử lý nghiêm sai phạm
Bộ Y tế vừa có văn bản gửi UBND các tỉnh, thành phố trực thuộc Trung ương về việc tăng cường công tác phòng chống ngộ độc thực phẩm
Theo đó, Bộ Y tế đề nghị UBND dân các tỉnh, thành phố trực thuộc Trung ương kiên quyết xử lý nghiêm, đình chỉ hoạt động cơ sở không đảm bảo điều kiện an toàn thực phẩm.
 |
| Bộ Y tế nêu rõ, khi xảy ra ngộ độc thực phẩm phải nhanh chóng cấp cứu, điều trị kịp thời cho bệnh nhân, truy xuất nguồn gốc thực phẩm, nguyên liệu thực phẩm đến cùng; xử lý nghiêm sai phạm. |
Đồng thời tăng cường công tác thanh tra, kiểm tra, giám sát an toàn thực phẩm, kiên quyết xử lý nghiêm và đình chỉ hoạt động đối với các cơ sở không đảm bảo điều kiện an toàn thực phẩm, cơ sở không có Giấy chứng nhận đủ điều kiện an toàn thực phẩm (đối với cơ sở thuộc đối tượng phải cấp);
Tập trung vào đối tượng là cơ sở sản xuất thực phẩm ăn ngay, thức ăn đường phố, các cơ sở kinh doanh nước giải khát, nước đá, các cơ sở kinh doanh dịch vụ ăn uống, bếp ăn tập thể tại các trường học, bệnh viện, khu công nghiệp, khu chế xuất...
Chú ý kiểm soát chất lượng an toàn thực phẩm đối với các loại lương thực, thực phẩm, nước uống do các tổ chức, cá nhân làm từ thiện, hoặc hỗ trợ người dân trong mùa nắng nóng, mùa mưa, lũ nhằm đảm bảo không để các sản phẩm bị hỏng, mốc, dập vỡ, không rõ nguồn gốc, hết hạn sử dụng... đến tay người dân.
Bộ Y tế đề nghị UBND các tỉnh, thành phố đẩy mạnh công tác tuyên truyền thường xuyên liên tục các biện pháp bảo đảm an toàn thực phẩm trong sản xuất, chế biến, kinh doanh và tiêu dùng thực phẩm, phù hợp với đặc điểm của địa phương (sử dụng tiếng dân tộc đối với vùng đồng bào dân tộc, chú ý cả các vùng sâu, vùng xa).
"Tuyên truyền để người dân không thu hái, đánh bắt, kinh doanh, sử dụng các động thực vật độc như nấm độc, côn trùng lạ, độc, cá nóc, so biển, ốc lạ, cây, quả lạ...; không sử dụng gia súc, gia cầm chết bệnh, chết không rõ nguyên nhân làm thức ăn hoặc chế biến thực phẩm;
Thực hiện ăn chín, uống chín, nước sử dụng để ăn uống, chế biến thực phẩm phải đảm bảo sạch hoặc được khử trùng, đặc biệt là trong thời gian nắng nóng, mưa, lũ"- Văn bản của Bộ Y tế lưu ý.
Đối với các vùng có nguy cơ chịu ảnh hưởng của bão, lũ cao, Bộ Y tế nhấn mạnh cần theo dõi các dự báo, diễn biến tình hình bão, lũ trên địa bàn và chủ động kế hoạch dự trữ các loại lương thực, thực phẩm chế biến sẵn, nước uống đóng chai, các loại vitamin, thuốc men, các hóa chất sát khuẩn của ngành y tế.
Bộ Y tế nêu rõ, khi xảy ra vụ ngộ độc thực phẩm, nhanh chóng tổ chức cấp cứu, điều trị kịp thời cho bệnh nhân, hạn chế tối đa ảnh hưởng đến sức khỏe, tính mạng người dân, đồng thời phải đình chỉ ngay hoạt động của cơ sở gây ngộ độc thực phẩm, yêu cầu khắc phục đúng quy định trước khi hoạt động trở lại;
Điều tra, lấy mẫu thực phẩm, bệnh phẩm để xác định rõ nguyên nhân và tiến hành truy xuất nguồn gốc thực phẩm, nguyên liệu thực phẩm đến cùng; xử lý nghiêm các vi phạm quy định về an toàn thực phẩm, công khai kết quả để cảnh báo cho cộng đồng.
Năm chính sách tạo bước phát triển mới cho ngành Dược
Dự thảo Luật sửa đổi, bổ sung một số điều của Luật Dược được xây dựng với 5 trụ cột chính là tăng cường hơn nữa việc cung ứng đủ, kịp thời thuốc có chất lượng cho nhu cầu phòng bệnh, chữa bệnh của người dân.
Bảo đảm cung ứng đủ, kịp thời thuốc đáp ứng yêu cầu an ninh, quốc phòng, khắc phục hậu quả thiên tai, phòng chống dịch bệnh trong tình hình mới.
Nâng cao hiệu quả quản lý xuất khẩu, nhập khẩu thuốc, nguyên liệu làm thuốc phù hợp với tình hình phát triển kinh tế - xã hội và thông lệ quốc tế.
Đẩy mạnh phát triển công nghiệp dược, ưu tiên nghiên cứu, tiếp nhận chuyển giao công nghệ và sản xuất thuốc phát minh, thuốc công nghệ cao, thuốc/nguyên liệu thuốc sinh học, thuốc dược liệu được tiêu chuẩn hóa, nguyên liệu từ nguồn dược liệu sẵn có trong nước. Và tổ chức, sắp xếp lại hệ thống kinh doanh, phân phối thuốc, nguyên liệu làm thuốc đáp ứng tình hình phát triển kinh tế - xã hội và hội nhập quốc tế.
Nội dung xuyên suốt tại 5 chính sách nêu trên nhằm giải quyết kịp thời những khó khăn, vướng mắc từ thực tiễn phòng, chống đại dịch và các vấn đề cấp bách cần tháo gỡ ngay để bảo đảm cung ứng đủ thuốc khám bệnh, chữa bệnh cho nhân dân;
Đồng thời đổi mới mạnh mẽ quy trình, thủ tục hành chính theo hướng cắt giảm tối đa thủ tục hành chính cho người dân và doanh nghiệp, tạo điều kiện thuận lợi tối đa cho doanh nghiệp nhưng vẫn bảo đảm chất lượng thuốc; đẩy mạnh phân cấp, phân quyền gắn với tăng cường trách nhiệm các cấp, các ngành.
Được biết, tình trạng thiếu thuốc chữa bệnh thời gian qua liên quan khá lớn đến việc cấp phép mới, gia hạn đăng ký lưu hành thuốc, nguyên liệu làm thuốc.
Vì vậy theo đại diện Bộ Y tết, Dự thảo Luật Dược sửa đổi đã đơn giản hóa hồ sơ gia hạn, thay đổi, bổ sung giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc. Tinh giản thủ tục hành chính, giảm thời gian gia hạn, cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc.
Về hồ sơ, trình tự, thủ tục gia hạn hiệu lực giấy đăng ký lưu hành đối với thuốc, nguyên liệu làm thuốc: Khoản 1 Điều 56 Luật Dược 2016 quy định tất cả các thuốc sau khi hết hạn hiệu lực Giấy đăng ký lưu hành, đều phải nộp lại hồ sơ gia hạn và các hồ sơ này đều phải trải qua quá trình thẩm định, xét duyệt của Hội đồng tư vấn cấp Giấy đăng ký lưu hành. Quy định này của Luật Dược đã góp phần giúp cho việc quản lý thuốc có chất lượng, an toàn và hiệu quả.
Tuy nhiên, quy định chỉ phù hợp với các thuốc trong quá trình lưu hành có vấn đề về chất lượng hoặc an toàn cần phải đánh giá lại trước khi gia hạn hiệu lực giấy đăng ký lưu hành.
Bên cạnh đó, tại dự thảo Luật Dược sửa đổi, ban soạn thảo đã đề xuất quy định các trường hợp gia hạn, thay đổi, bổ sung Giấy đăng ký lưu hành không phải thông qua Hội đồng tư vấn cấp Giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc hoặc không phải phê duyệt.
Giảm thời gian giải quyết hồ sơ từ 3 tháng xuống còn 15 ngày làm việc đối với hồ sơ thay đổi, bổ sung chỉ cần công bố.
Bổ sung quy định cho phép cơ sở được tiếp tục sử dụng giấy đăng ký lưu hành sau khi hết hiệu lực và đã nộp hồ sơ gia hạn theo quy định đến khi được gia hạn hoặc có văn bản của Bộ Y tế.
Bổ sung quy định cho phép thay thế CPP bằng giấy tờ pháp lý chứng minh thuốc được cấp phép trong trường hợp đáp ứng nhu cầu phòng, chống dịch bệnh…
Khoản 3 Điều 56 Luật Dược quy định hồ sơ gia hạn hiệu lực Giấy đăng ký lưu hành phải nộp 6 loại tài liệu, chủ yếu là các tài liệu về hành chính.
Theo ban soạn thảo, quy định nộp 6 tài liệu trong bối cảnh việc cấp phép lưu hành lần đầu trước đây chưa áp dụng hệ thống cấp giấy phép lưu hành thuốc trực tuyến (online).
Hiện nay, Bộ Y tế đã triển khai hệ thống cấp phép trực tuyến và trong thời gian tới sẽ liên thông cơ sở dữ liệu dược quốc gia thì hoàn toàn tra cứu lại được các tài liệu này nên không cần thiết phải yêu cầu nộp lại.
Việc phải nộp nhiều tài liệu trong hồ sơ đã dẫn đến lãng phí thời gian, nguồn lực cho doanh nghiệp khi chuẩn bị hồ sơ cũng như tạo áp lực cho cơ quan quản lý trong việc phải thẩm định, xét duyệt hồ sơ.
Ngoài nội dung đẩy nhanh tiến độ gia hạn đăng ký lưu hành thuốc, nguyên liệu làm thuốc, Dự thảo Luật Dược đã bổ sung nhiều chính sách, nhất là chính sách ưu đãi đầu tư, hỗ trợ đầu tư đối với các hoạt động nghiên cứu, chuyển giao công nghệ, đầu tư sản xuất thuốc, nguyên liệu làm thuốc.
Theo nhiều doanh nghiệp dược phẩm, các chính sách ưu đãi đầu tư cần thể hiện tính đột phá, đủ mạnh, đồng bộ về đầu tư, đào tạo, nghiên cứu khoa học, thương mại hóa sản phẩm, xúc tiến thương mại, xây dựng, quảng bá thương hiệu Việt Nam, phát triển chuỗi giá trị, liên kết phát triển dược, nhất là phát triển dược liệu, phát triển vùng trồng dược liệu quý, sản xuất thuốc từ nguồn dược liệu sẵn có trong nước…
Đối với vấn đề cung ứng dược liệu, nêu thực tế vừa qua có hiện trạng không cung ứng kịp thời thuốc và dược phẩm, cơ chế còn vướng mắc, các đại biểu đề nghị cần có những điều khoản quy định rõ về vấn đề này, tạo điều kiện thuận lợi cho việc tiếp cận thuốc trong các điều kiện, hoàn cảnh đặc biệt.
Đồng thời, đề xuất bổ sung “thuốc điều trị bệnh hiếm gặp” vào đối tượng được ưu tiên về trình tự, thủ tục đăng ký lưu hành, cấp phép nhập khẩu; tiếp tục rà soát và thể hiện thời gian thực hiện thủ tục hành chính được rút ngắn cho quy trình thẩm định cấp phép đối với hồ sơ đăng ký lưu hành thuốc hiếm, vắc- xin đã được Tổ chức Y tế thế giới tiền thẩm định, thuốc đã được thử lâm sàng tại Viêt Nam;
Ngoài ra, có chính sách ưu đãi về nguồn lực cho hoạt động quản lý nhà nước về dược, đáp ứng đủ nhân lực có trình độ chuyên môn cao, các chuyên gia có kinh nghiệm trong công tác quản lý và kỹ thuật;…
Thời gian vừa qua, trước những yêu cầu và đòi hỏi cấp bách từ thực tiễn, hệ thống pháp luật về dược đang tồn tại đã bộc lộ một số hạn chế, bất cập như: Một số quy định liên quan về đăng ký lưu hành thuốc, nguyên liệu làm thuốc chưa phù hợp chủ trương cải cách hành chính; Một số quy định về quản lý chất lượng thuốc chưa phù hợp chủ trương phân cấp quản lý;
Một số chính sách phát triển công nghiệp dược chưa tạo được bước đột phá cho công nghiệp dược Việt Nam trong tình hình mới; Một số quy định về quản lý giá thuốc chưa phù hợp thực tiễn cũng như pháp luật về giá mới được ban hành;
Ngoài ra một số quy định về kinh doanh, loại hình kinh doanh dược cần điều chỉnh để đáp ứng sự phát triển và xu thế hội nhập; Một số quy định liên quan đến thông tin, quảng cáo thuốc tạo gánh nặng cho doanh nghiệp, chưa phù hợp với chủ trương cải cách hành chính;
Một số quy định về đăng ký, sản xuất, xuất, nhập khẩu và cung ứng thuốc không phù hợp hoặc chưa được quy định để thực hiện trong trường hợp khẩn cấp đáp ứng nhu cầu phòng, chống dịch bệnh, an ninh, quốc phòng.
Do đó, để khắc phục những hạn chế, bất cập nêu trên, việc xây dựng Dự án Luật sửa đổi, bổ sung một số điều của Luật Dược là cần thiết.

-
Tin mới y tế ngày 8/5: Phẫu thuật thành công ca động kinh kháng thuốc nhờ công nghệ ECoG -
Bác sỹ của những "đường mổ vô hình" và giấc mơ y học Việt Nam -
Xuất hiện nhiều hình thức mạo danh MEDLATEC, khách hàng cần cảnh giác -
TP.HCM ghi nhận 4 ca tử vong do bệnh dại, ngành y tế tăng cường giám sát -
Loạt công nghệ điều trị nhãn khoa hiện đại được cập nhật tại Việt Nam -
Nhiều người dân vùng sâu vượt hàng chục km đi tiêm vắc-xin phòng dịch -
Lộ trình khám sức khỏe miễn phí cho toàn dân từ năm 2026
-
 Acecook Việt Nam khởi động dự án trồng 10.500 cây xanh tại tỉnh Quảng Trị - “Gieo mầm hạnh phúc - phủ xanh tương lai”
Acecook Việt Nam khởi động dự án trồng 10.500 cây xanh tại tỉnh Quảng Trị - “Gieo mầm hạnh phúc - phủ xanh tương lai” -
 Giao lưu nhân dân tại Đồng Nai chào mừng 50 năm quan hệ Việt Nam - Thái Lan
Giao lưu nhân dân tại Đồng Nai chào mừng 50 năm quan hệ Việt Nam - Thái Lan -
 CEO Anh Tuấn và Untra Group - Kiến tạo hệ sinh thái ESG cho doanh nghiệp Việt
CEO Anh Tuấn và Untra Group - Kiến tạo hệ sinh thái ESG cho doanh nghiệp Việt -
 Fenica - Căn hộ TOD dành riêng cho giới trẻ chính thức chào sân tại Đông Bắc TP.HCM
Fenica - Căn hộ TOD dành riêng cho giới trẻ chính thức chào sân tại Đông Bắc TP.HCM -
 AMY GRUPO kỷ niệm 10 năm kiến tạo hệ sinh thái vật liệu xây dựng
AMY GRUPO kỷ niệm 10 năm kiến tạo hệ sinh thái vật liệu xây dựng -
SeABank thông báo mời thầu